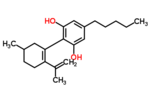
كانابيديول
| كانابيديول | |
|---|---|
| الاسم النظامي | |
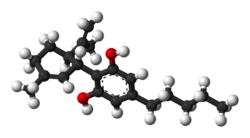
| 2-[(1R,6R)-6-آيزوبرينيل-3-ميثيل سيكلوهيكسين-2-إن-1-ويل]-5-بنتيل بنزين-1,3- ديول | |
| اعتبارات علاجية | |
| اسم تجاري | إبيديولكس |
| مرادفات | CBD, cannabidiolum, (−)-cannabidiol[1] |
| ASHPDrugs.com | أسماء الدواء الدولية |
| مدلاين بلس | a618051 |
| إدمان المخدرات | منخفض[2] |
| بيانات دوائية | |
| توافر حيوي | |
| عمر النصف الحيوي | 18–32 ساعة[5] |
| معرّفات | |
| CAS | 13956-29-1 |
| ك ع ت | None |
| بوب كيم | CID 644019 |
| IUPHAR | 4150 |
| ECHA InfoCard ID | 100.215.986 |
| درغ بنك | 09061 |
| كيم سبايدر | 24593618 |
| المكون الفريد | 19GBJ60SN5 |
| ChEBI | CHEBI:69478 |
| ChEMBL | CHEMBL190461 |
| ترادف | CBD, cannabidiolum, (−)-cannabidiol[1] |
| بيانات كيميائية | |
| الصيغة الكيميائية | C21H30O2 |
| الكتلة الجزيئية | 314.4636 |
| بيانات فيزيائية | |
| نقطة الانصهار | 66 °C (151 °F) |
| تعديل مصدري - تعديل | |
الكانابيديول[7] هو واحد من 113 على الأقل من الكانابينويدات النشطة الموجودة في نبات القنب.[8][9]، يعتبر الكانابيديول أحد الكانبينويدات الرئيسية؛ إذ يمثل ما يصل إلى 40% من مستخرج النبات.[10]
لا يسبب الكانبيديول أي تأثير سام مثل تلك الآثار التي يسببها رباعي هيدرو كانابينول الموجود في الماريجوانا، ولكن قد يكون له آثارمضادة القلق وتأثير مضاد للذهان.[11]
الأبحاث[عدل]

متلازمة درافيت (الملقبة بصرع الرمع العضلي الطفولي) هو شكل نادر من أشكال الصرع التي يصعب علاجها. وهو شكل كارثي من أشكال الصرع المستعصية التي تبدأ في مرحلة الطفولة. تبدأ النوبات في الظهور لأول مرة وتحدث لفترات طويلة، وفي السنة الثانية من الحياة تبدأ أنواع أخرى من النوبات في الظهور.[12] وقد أثار عدد من التقارير البارزة والمؤلفات الطبية الاهتمام في علاج متلازمة درافيت باستخدام الكانابيديول.[13] وقد صنف الكانابيديول تحت حالة دواء يتيم في الولايات المتحدة، لعلاج متلازمة درافيت التي ستسمح بدراستها.[14]
يتم تسويق بعض مستحضرات القنب التي تحتوي على الكانابيديول كمكملات غذائية (مكمل غذائي) ذات فعالية في علاج متلازمة درافيت. ويتم تسويق إحدى هذه المستحضرات تحت الاسم التجاري مستحضر شارلوت المستخرج من القنب.[15]
تسعى شركة غو للأدوية إلى الحصول على موافقة إدارة الأغذية والدواء على تسويق تركيبة سائلة للكانابيديول المشتق من نباتات القنب النقية تحت الاسم التجاري إبيديوليكس (الذي يحتوي على 99% كانابيديول وأقل من 0.10% من رباعي هيدرو كانابينول) كعلاج لمتلازمة درافيت. تم منح إبيديوليكس وضع المسار السريع وهو في مرحلة متأخرة من التجارب بعد نتائج مبكرة إيجابية لهذا الدواء..[13][16][17][18][19]
وذكر استعراض عام 2014 أن البعض قد زعم، على حد قولهم، أن الكانابيديول قد يكون تكون مفيدًا في مساعدة المصابين بالصرع. وذكرت المعلومات الواردة في الاستعراض أنه لا توجد آلية عمل ثابتة لهذا الغرضآلية عمل ولا توجد أدلة عالية الجودة في هذا المجال للوصول إلى تلك الاستنتاجات.
ويشير استعراض عام 2016 إلى أنه نظرًا لانخفاض دقة البيانات المتاحة، «لا يمكن استخلاص أي استنتاجات» بشأن فعالية الكانابيديول كعلاج للصرع.
مضاد للذهان[عدل]
توجد أدلة أولية على أن الكانبيديول له تأثير مضاد للذهان، ولكن لا تزال الأبحاث في هذا المجال محدودة.[20][21]
السلامة[عدل]
تمت دراسة سلامة استخدام الكانابيديول في البشر في دراسات صغيرة متعددة، مما يشير إلى أنه يمكن تحمله بجرعات تصل إلى 1500 ملغ / يوم (في حالة تناوله عن طريق الفم) أو 30 ملغ (في حالة إعطاءه عن طريق الوريد).[22]
الديناميكا الدوائية[عدل]
يتميز الكانبيديول بتقارب منخفض جدًا لمستقبلات الكانابينويد CB1 و CB2 ولكنه يعمل كمضاد غير مباشر لهذه المستقبلات.[23][24] ويمكن أن يحفز آثار رباعي هيدرو كانابينول عن طريق زيادة كثافة مستقبلات CB1 أو من خلال آلية أخرى تتعلق بمستقبلات CB1.[25] يمكن أن يمدد الكانابيديول أيضا مدة آثار رباعي هيدرو كانابينول عن طريق تثبيط إنزيمات سيتوكروم بي 450 CYP3A و CYP2C.[26]
وُجد أن الكانابيديول يعمل كمضاد لمستقبل GPR55، وهو مستقبل مقترن بالبروتين ج ومستقبلات القنب المفترضة التي يتم التعبير عنها في النواة الذنبية والبطامة في الدماغ.[27] وقد تبين أيضًا أنه يعمل كمنبه جزئي لمستقبلات 5-HT1A،[28] وقد يكون تلك الآلية مسؤولة عن التأثير المضاد للاكتئاب،[29][30] والمضاد للقلق،[30][31] والتأثير الواقي للجهاز العصبي[32][33] الخاص بالكانابيديول. كما يعتبر الكانبيديول أحد المغيرات المشوهة لمستقبلات μ- و δ-الأفيونية أيضًا. [35] وتُعزى الآثار الدوائية للكانابيديول بالإضافة إلى ذلك إلى تنبيه مستقبلات PPAR وإدخال الكالسيوم داخل الخلايا.[10]
وتشير الأبحاث إلى أن الكانابيديول قد يظهر بعض آثاره الدوائية من خلال تثبيطه للأحماض الدهنية أميد هيدرولاز، مما قد يزيد بدوره من مستويات إندوكانابينويدس، مثل أنانداميد، التي ينتجها الجسم.[10] كما تم التكهن بأن بعض منتجات الأيض للكانابيديول لها تأثيرات دوائية تساهم في النشاط البيولوجي للكانابيديول.[34]
التفاعلات الدوائية[عدل]
توجد بعض الأدلة الطبية التي تشير إلى أن الكانابيديول قد يقلل من تخلص الجسم من رباعي هيدرو كانابينول، مما يسبب زيادة متواضعة في تركيزات رباعي هيدرو كانابينول في البلازما مما أدى إلى كمية أكبر من رباعي هيدرو كانابينول المتاح للمستقبلات، وزيادة تأثير رباعي هيدرو كانابينول بطريقة تعتمد على الجرعة.[35][36] على الرغم من هذا، تشير الأدلة المتاحة في البشر إلى أنه لا يوجد أي تأثير كبير للكانابيديول على مستويات رباعي هيدرو كانابينول في البلازما.[37]
المستحضرات الداوائية[عدل]
نابيكسيمولس (أوسان، والاسم التجاري ساتكس) هو رزاز يستنشق عن طريق الفم التي يحتوي على نسبة 1: 1 تقريبًا من الكانابيديول ورباعي هيدرو كانابينول تمت الموافقة عليه من قبل السلطات الكندية في عام 2005 لتخفيف الألم المرتبط بالتصلب المتعدد..[38][39] كما صُنف إبيديوليكس، وهو دواء يحتوي على الكانابيديول كعنصرنشط، تحت حالة الأدوية اليتيمة في الولايات المتحدة لعلاج متلازمة درافيت في يوليو عام 2015.[40]
إبيديوليكس هو مستحضر زيتي دوائي من الكانابيديول المستخرج من القنب والذي يخضع لتجارب سريرية لعلاج متلازمات الصرع المستعصية.[41]
الكيمياء[عدل]
الكانابيديول غير قابل للذوبان في الماء ولكنه قابل للذوبان في المذيبات العضوية مثل البنتان. يأخذ الكانبيديول في درجة حرارة الغرفة، شكل بلوري صلب عديم اللون.[42] يتأكسد الكانبيديول في الوسط القلوي القوي ووجود الهواء، إلى كينون.[43] كما يتحول الكانابيديول في الأوساط الحمضية إلى رباعي هيدرو كانابينول.[44] وقد تم تخليق الكانابيديول من قبل عدة مجموعات بحثية.[45][46][47]
التخليق الحيوي[عدل]
ينتج القنب كانانبيديول حمض الكربوكسيل من خلال نفس مسار التمثيل الغذائي لرباعي هيدرو كانابينول، حتى الخطوة الأخيرة، حيث يحفز إنزيم مخلق الكانابيديول أ التفاعل لتكوين الكانابيديول بدلًا من إنزيم مُخلق رباعي هيدرو كانابينول.[48]

النظائر[عدل]

الثقافة والمجتمع[عدل]
المصادر الطبيعية[عدل]
وقد أدى التكاثر الانتقائي من قبل المزارعين في الولايات المتحدة الأمريكية إلى خفض كبير في محتوى القنب للكانابيديول؛ إذ يفضل الزبائن الأصناف التي تذهب العقل بصورة أكبر لارتفاع نسبة رباعي هيدروكانابينول، وانخفاض محتوى الكانبيديول الموجود فيها.[50] ولتلبية متطلبات مرضى القنب الطبي، يقوم المزارعون حاليًا بتطوير المزيد من السلالات السائدة التي تحتوي على الكانبيديول.[51]
المصادر المزيفة[عدل]
ذكرت رابطة صناعات القنب في عام 2014 أن زيت بذور القنب يحتوي على الكانبيديول بنسبة أقل من 25 جزءا في المليون، وبالتالي لا يعتبر زيت القنب مصدرًا للكانبيديول يمكن استخدامه في علاجات الصرع.[52]
الحالة القانونية[عدل]
لا يبدو أن الكانبيديول يتمتع بأي آثار نفسية «عالية» مثل تلك التي يسببها رباعي هيدروكانابينول الموجود في الماريجوانا، ولكن قد يكون له آثار مضادة للقلق وتأثيرات مضادة للذهان.[11] مع تكشف المشهد القانوني والفهم حول الاختلافات في شبائه القنب الطبية، سيكون من المهم التمييز بين «الماريجوانا الطبية» (مع درجات متفاوتة من التأثيرات العقلية والقصور الوظيفي) - من «الكانبيديول الطبي».[11][53]
تم العثور على سلالات مختلفة من «الماريجوانا الطبية» لديها مجموعة كبيرة ومتنوعة في نسب الكانبيديول ورباعي هيدروكانابينول ومن المعروف أنها تحتوي على غيرها من شبائه القنب غير المؤثرة على القوى العقلية. ومع ذلك تعتبر كمية رباعي هيدروكانابينول هي التي تحدد كيميائيًا ما إذا كانت المواد النباتية المستخدمة لأغراض استخراج الكانبيديول تعتبر قنب، أو تعتبر ماريجوانا.
تشتق الماريجوانا ذات التأثير النفسي، بغض النظر عن محتواها من الكانابيديول، من زهرة (أو برعم نباتات القنب. أما القنب غير النفساني (والذي عادةً ما يُطلق عليه اسم القنب الصناعي)، بغض النظر عن محتواه من الكانبيديول، فهو يُشتق من أي جزء من نبات القنب، سواء كان متناميًا أم لا، يحتوي على تركيز من رباعي هيدروكانابينول لا يزيد عن ثلاثة أعشار واحد في المائة (0.3٪) على أساس الوزن الجاف. وهناك معايير معينة مطلوبة للزراعة القانونية وإنتاج القنب. يسجل برنامج القنب الصناعي كولورادو مزارعي القنب الصناعي وعينات المحاصيل للتحقق من أن تركيزات رباعي هيدروكانابينول لا تتجاوز 0.3% على أساس الوزن الجاف.[54]
الأمم المتحدة[عدل]
لا يُدرج الكانابيديول صمن المواد المحظورة لتأثيرها على القوى العقلية.
الولايات المتحدة[عدل]
رفع إحدى برامج قناة سي إن إن CNN التي عرضت مستحضرات شارلوت المستخرجة من القنب في عام 2013 من الطلب على زراعة سلالات الكانابيديول السائدة في جميع أنحاء الولايات المتحدة. شُرعت التشريعات في ولاية كنتاكي في عام 2013 لتعزيز زراعة القنب في الدولة كأحد برامج التنمية الاقتصادية لمساعدة مزارعي التبغ الذين فقدوا أسواق محاصيلهم. ضغطت الولاية وفازت بمرادها بإقرار قانون تم التصديق عليه لإنتاج القنب في ولايات مثل ولاية كنتاكي عام 2014.[55][56][57]
واعتبارًا من عام 2017، قنّنت 31 ولاية على الأقل إنتاج القنب الصناعي، بما في ذلك على سبيل المثال: كاليفورنيا، كولورادو، إنديانا، مين، مونتانا وكارولينا الشمالية، داكوتا الشمالية، ولاية أوريغون، ولاية كارولينا الجنوبية، تينيسي، فيرمونت، وفرجينيا الغربية. كما شرعت العديد من الولايات الأخرى قوانين يجيز زراعة القنب الصناعي للمشاريع التجريبية أو الدراسات، بما في ذلك: كونيتيكت وديلاوير وهاواي، إلينوي وكنتاكي ونبراسكا، ويوتا. بالإضافة إلى ذلك، دعمت الرابطة الوطنية لإدارات الدولة للزراعة والمؤتمر الوطني للمجالس التشريعية في الولايات كل القرارات التي اتخذت لدعم التنقيحات التي أدخلت على القواعد الاتحادية واللوائح التي تجيز الإنتاج التجاري من القنب الصناعي.[58][59][60]
في ولاية يوتا، يُعرض ممتلكي نبات القنب السائد المحتوي على الكانابيديول للعقوبات ى لحيازتهم أو استخدامهم لمستخلص القنب تحت المواد الخاضعة للرقابة القانون إذا لم يحصلوا للحصول على تصريح من أحد أخصائي الأعصاب يسمح باستخراج القنب.[61] يحدد أخصائي الأعصاب إذا ما كان المريض لديه علامات الصرع المستعصي أو ما إذا كان المريض قد يستفيد من استخدام مستخلص القنب. يشترط القانون على طبيب الأعصاب الحفاظ على ونقل البيانات لقاعدة بيانات الإدارة الصحية في يوتا تحت قسم تقييمات الحالات العصبية.[62] كما تتطلب الحيازة الفردية لمستخلص القنب الحصول على شهادة تسمح للبائع ببيع مستخلصات القنب.[63]
أستراليا[عدل]
تحتوي الوصفة الطبية (جدول 4) للاستخدام العلاجي على (2.0٪) أو أقل من المواد المخدرة الأخرى الموجودة عادةً في القنب رباعي هيدرو كانبينول.[64]
كندا[عدل]
يُصنف الكانابيديول كدواء مُدرج في الجدول الثاني في كندا. ولا يتم صرفه إلا مع الوصفات الطبية.[65]
أوروبا[عدل]
يُدرج الكانابيديول في قاعدة بيانات مستحضرات التجميل الاتحاد الأوروبي المكون.[66]
يُدرج د الكانابيديول في كتالوج الاتحاد الأوروبي للأغذية الغريبة.[67] هذه القائمة لا تنطبق إلا على الكانبيديول المعزول أو الاصطناعي، وليس على مستخرجات القنب الخام أو الصبغات التي تحتوي على الكانابيديول بشكل طبيعي.[68]
أصدرت الرابطة الأوروبية للقنب الصناعي ورقة تقترح الإطار التنظيمي في الاتحاد الأوروبي.[69]
عدة أنواع القنب الصناعية يمكن زراعتها بشكل قانوني في أوروبا الغربية. مجموعة متنوعة فحص ب «فيدورا 17» لديه ملف القنب باستمرار حوالي 1% الكانابيديول مع رباعي هيدروكانابينول أقل من 0.1٪.[69]
على الرغم من أن منظمة الصحة العالمية أدرجت الكانبيديول في قائمة الأسماء الدولية غير مسجلة الملكية للمستحضرات الصيدلانية في 30 يونيو 2016، إلا أن الإصدارات الفرنسية والإسبانية ذكرت خطأ التأثير التنبيهي للكانابيديول على مستقبلات القتب في حين أفادت الإصدارات الإنجليزية أن الكانبيديول هو مضاد لمستقبلات القنب.
السويد[عدل]
لا يصنف الكانابيديول في السويد.
يستخدم ساتيفكس (وهو منتج يحتوي على الكانابيديول ورباعي هيدرو كانابينول) كوصفة طبية متوفرة للتخفيف من التشنج الشديد بسبب التصلب المتعدد.[70][71]
المملكة المتحدة[عدل]
تستخدم المنتجات الت تحتوي على الكانابيديول ورباعي هيدرو كانابينول كوصفة طبية متوفرة للتخفيف من التشنج الشديد بسبب التصلب المتعدد (حيث لم تظهر مضادات التشنج الأخرى أي فعالية).[72]
اعتبارًا من 31 ديسمبر 2016، تم تصنيف المنتجات التي تحتوي على الكانابيديول التي يتم تسويقه كأدوية تنظمها الهيئة التنظيمية في المملكة المتحدة، والأدوية ووكالة تنظيم منتجات الرعاية الصحية (MHRA) والتي لا يمكن تسويقها دون موافقة الجهات التنظيمية دون وصفات طبية أو لغير الأغراض الطبية.[73]
سويسرا[عدل]
في حين لا يزال رباعي هيدرو كانابينول غير قانوني، لا يُدرج الكانابيديول تحت قوانين المخدرات السويسرية لأنه لا ينتج تأثير منشط مقارنةً برباعي هيدرو كانابينول.[74] وبناءُا عليه، يمكن أن تباع مشتقات القنب المحتوية على الكانابيديول بشكل قانوني طالما أنها ل تحتوي على أقل من 1% من رباعي هيدرو كانابينول.[75]
مراجع[عدل]
- ^ "cannabidiol (CHEBI:69478)". ebi.ac.uk. مؤرشف من الأصل في 2021-05-12. اطلع عليه بتاريخ 2019-02-12.
- ^ "Federal Register :: Request Access". unblock.federalregister.gov. مؤرشف من الأصل في 2024-03-07. اطلع عليه بتاريخ 2024-03-10.
- ^ Perucca E، Bialer M (5 يونيو 2020). "Critical Aspects Affecting Cannabidiol Oral Bioavailability and Metabolic Elimination, and Related Clinical Implications". CNS Drugs. ج. 34 ع. 8: 795–800. DOI:10.1007/s40263-020-00741-5. PMID:32504461. S2CID:219313952.
- ^ Scuderi C، Filippis DD، Iuvone T، Blasio A، Steardo A، Esposito G (مايو 2009). "Cannabidiol in medicine: a review of its therapeutic potential in CNS disorders". Phytotherapy Research (Review). ج. 23 ع. 5: 597–602. DOI:10.1002/ptr.2625. PMID:18844286. S2CID:21836765. مؤرشف من الأصل في 2021-04-11. اطلع عليه بتاريخ 2020-05-22.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعdevinsky - ^ DEA News Release, DEA Eases Requirements for FDA Approved Clinical Trials on Cannabidiol (December 23, 2015) ("CBD is a Schedule I controlled substance as defined under the CSA."), https://www.dea.gov/press-releases/2015/12/23/dea-eases-requirements-fda-approved-clinical-trials-cannabidiol Joseph T. Rannazzisi Deputy Assistant Administrator Drug Enforcement Administration Before the Caucus on International Narcotics Control, United States Senate, at 2 (June 24, 2015) (CBD is a Schedule I drug.); انظر أيضًا Frank Robison, Elvira Strehle-Henson, Cannabis Laws and Research at Colorado Institutions of Higher Education, COLO. LAW., OCTOBER 2015, AT 73, 76 ("[T]the DEA's position on CBD is clear—it is a Schedule I substance."). نسخة محفوظة 10 أبريل 2020 على موقع واي باك مشين.
- ^ "International Nonproprietary Names for Pharmaceutical Substances (INN)" (PDF). WHO Drug Information. ج. 30 ع. 2: 241. 2016. مؤرشف من الأصل (PDF) في 2018-02-05.
- ^ Borgelt LM، Franson KL، Nussbaum AM، Wang GS (فبراير 2013). "The pharmacologic and clinical effects of medical cannabis". Pharmacotherapy (Review). ج. 33 ع. 2: 195–209. DOI:10.1002/phar.1187. PMID:23386598.
- ^ Aizpurua-Olaizola, Oier; Soydaner, Umut; Öztürk, Ekin; Schibano, Daniele; Simsir, Yilmaz; Navarro, Patricia; Etxebarria, Nestor; Usobiaga, Aresatz (2 Feb 2016). "Evolution of the Cannabinoid and Terpene Content during the Growth ofCannabis sativaPlants from Different Chemotypes". Journal of Natural Products (بالإنجليزية). 79 (2): 324–331. DOI:10.1021/acs.jnatprod.5b00949. PMID:26836472.
- ^ أ ب ت Campos AC، Moreira FA، Gomes FV، Del Bel EA، Guimarães FS (ديسمبر 2012). "Multiple mechanisms involved in the large-spectrum therapeutic potential of cannabidiol in psychiatric disorders". Philos. Trans. R. Soc. Lond., B, Biol. Sci. (Review). ج. 367 ع. 1607: 3364–78. DOI:10.1098/rstb.2011.0389. PMC:3481531. PMID:23108553.
- ^ أ ب ت Iseger TA، Bossong MG (2015). "A systematic review of the antipsychotic properties of cannabidiol in humans". Schizophr. Res. ج. 162 ع. 1–3: 153–61. DOI:10.1016/j.schres.2015.01.033. PMID:25667194.
- ^ "What is Dravet Syndrome?". Dravetfoundation.org. 20 يونيو 2014. مؤرشف من الأصل في 2016-10-28. اطلع عليه بتاريخ 2016-12-04.
- ^ أ ب Melville، Nancy A. (14 أغسطس 2013)، Seizure Disorders Enter Medical Marijuana Debate، مدسكيب.، مؤرشف من الأصل في 2019-06-11، اطلع عليه بتاريخ 2014-01-14
{{استشهاد}}: استعمال الخط المائل أو الغليظ غير مسموح:|ناشر=(مساعدة) - ^ "Cannabis-Derived Dravet Syndrome Drug Gets US Orphan Drug Approval". 18 نوفمبر 2013. مؤرشف من الأصل في 2018-06-26. اطلع عليه بتاريخ 2015-07-21.
- ^ Maa، Edward؛ Figi، Paige (2014). "The case for medical marijuana in epilepsy". Epilepsia. ج. 55 ع. 6: 783–786. DOI:10.1111/epi.12610. ISSN:0013-9580.
- ^ Throckmorton، Douglas (24 يونيو 2015). "Cannabidiol: Barriers to Research and Potential Medical Benefits". إدارة الغذاء والدواء (الولايات المتحدة). إدارة الغذاء والدواء (الولايات المتحدة). مؤرشف من الأصل في 2018-01-25. اطلع عليه بتاريخ 2015-12-15.
- ^ Gloss D، Vickrey B (13 يونيو 2012). "Cannabinoids for epilepsy". Cochrane Database Syst Rev (Review). ج. 6 ع. 6: CD009270. DOI:10.1002/14651858.CD009270.pub2. PMID:22696383.
- ^ Devinsky، Orrin (2015). "Efficacy and Safety of Epidiolex (Cannabidiol) in Children and Young Adults with Treatment-Resistant Epilepsy". Annual Meeting Abstracts. American Epilepsy Society. مؤرشف من الأصل في 2019-08-29. اطلع عليه بتاريخ 2015-12-13.
- ^ Angus، Chen (8 ديسمبر 2015). "Marijuana's Main Ingredient, Cannabidiol, May Be An Effective Way To Treat Epilepsy". Medical Daily. مؤرشف من الأصل في 2018-11-18. اطلع عليه بتاريخ 2015-12-14.
- ^ Leweke FM، Mueller JK، Lange B، Rohleder C (2016). "Therapeutic Potential of Cannabinoids in Psychosis". Biol. Psychiatry. ج. 79 ع. 7: 604–12. DOI:10.1016/j.biopsych.2015.11.018. PMID:26852073. مؤرشف من الأصل في 2019-12-13.
- ^ Schubart CD، Sommer IE، Fusar-Poli P، de Witte L، Kahn RS، Boks MP (2013). "Cannabidiol as a potential treatment for psychosis". European Neuropsychopharmacology. ج. 24 ع. 1: 51–64. DOI:10.1016/j.euroneuro.2013.11.002. PMID:24309088.
- ^ Devinsky O، Cilio MR، Cross H، Fernandez-Ruiz J، French J، Hill C، وآخرون (يونيو 2014). "Cannabidiol: pharmacology and potential therapeutic role in epilepsy and other neuropsychiatric disorders". Epilepsia. ج. 55 ع. 6: 791–802. DOI:10.1111/epi.12631. PMC:4707667. PMID:24854329.
- ^ Mechoulam R، Peters M، Murillo-Rodriguez E، Hanus LO (أغسطس 2007). "Cannabidiol—recent advances". Chem. Biodivers. (Review). ج. 4 ع. 8: 1678–92. DOI:10.1002/cbdv.200790147. PMID:17712814.
- ^ Pertwee RG (2008). "The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: Δ9-tetrahydrocannabinol, cannabidiol and Δ9-tetrahydrocannabivarin". British Journal of Pharmacology. ج. 153 ع. 2: 199–215. DOI:10.1038/sj.bjp.0707442. PMC:2219532. PMID:17828291.
- ^ Hayakawa K، Mishima K، Hazekawa M، Sano K، Irie K، Orito K، Egawa T، Kitamura Y، Uchida N، Nishimura R، Egashira N، Iwasaki K، Fujiwara M (2008). "Cannabidiol potentiates pharmacological effects of Δ9-tetrahydrocannabinol via CB1 receptor-dependent mechanism". Brain Research. ج. 1188: 157–164. DOI:10.1016/j.brainres.2007.09.090. PMID:18021759.
- ^ Alchimia Blog, Cannabinoids and their medicinal properties نسخة محفوظة 06 يوليو 2017 على موقع واي باك مشين.
- ^ Ryberg E، Larsson N، Sjögren S، Hjorth S، Hermansson NO، Leonova J، Elebring T، Nilsson K، Drmota T، Greasley PJ (2007). "The orphan receptor GPR55 is a novel cannabinoid receptor". British Journal of Pharmacology. ج. 152 ع. 7: 1092–101. DOI:10.1038/sj.bjp.0707460. PMC:2095107. PMID:17876302.
- ^ Russo EB، Burnett A، Hall B، Parker KK (أغسطس 2005). "Agonistic properties of cannabidiol at 5-HT1a receptors". Neurochemical Research. ج. 30 ع. 8: 1037–43. DOI:10.1007/s11064-005-6978-1. PMID:16258853.
- ^ Zanelati TV، Biojone C، Moreira FA، Guimarães FS، Joca SR (يناير 2010). "Antidepressant-like effects of cannabidiol in mice: possible involvement of 5-HT1A receptors". British Journal of Pharmacology. ج. 159 ع. 1: 122–8. DOI:10.1111/j.1476-5381.2009.00521.x. PMC:2823358. PMID:20002102.
- ^ أ ب Resstel LB، Tavares RF، Lisboa SF، Joca SR، Corrêa FM، Guimarães FS (يناير 2009). "5-HT1A receptors are involved in the cannabidiol-induced attenuation of behavioural and cardiovascular responses to acute restraint stress in rats". British Journal of Pharmacology. ج. 156 ع. 1: 181–8. DOI:10.1111/j.1476-5381.2008.00046.x. PMC:2697769. PMID:19133999.
- ^ Campos AC، Guimarães FS (أغسطس 2008). "Involvement of 5HT1A receptors in the anxiolytic-like effects of cannabidiol injected into the dorsolateral periaqueductal gray of rats". Psychopharmacology. ج. 199 ع. 2: 223–30. DOI:10.1007/s00213-008-1168-x. PMID:18446323.
- ^ Mishima K، Hayakawa K، Abe K، Ikeda T، Egashira N، Iwasaki K، Fujiwara M (مايو 2005). "Cannabidiol prevents cerebral infarction via a serotonergic 5-hydroxytryptamine1A receptor-dependent mechanism". Stroke; a Journal of Cerebral Circulation. ج. 36 ع. 5: 1077–82. DOI:10.1161/01.STR.0000163083.59201.34. PMID:15845890.
- ^ Hayakawa K، Mishima K، Nozako M، Ogata A، Hazekawa M، Liu AX، Fujioka M، Abe K، Hasebe N، Egashira N، Iwasaki K، Fujiwara M (مارس 2007). "Repeated treatment with cannabidiol but not Delta9-tetrahydrocannabinol has a neuroprotective effect without the development of tolerance". Neuropharmacology. ج. 52 ع. 4: 1079–87. DOI:10.1016/j.neuropharm.2006.11.005. PMID:17320118.
- ^ Ujváry I، Hanus L (2014). "Human metabolites of cannabidiol: a review on their formation, biological activity, and relevance in therapy". Cannabis and Cannabinoid Research. ج. 1 ع. 1: 90–101. DOI:10.1089/can.2015.0012.
- ^ Bornheim LM، Kim KY، Li J، Perotti BY، Benet LZ (أغسطس 1995). "Effect of cannabidiol pretreatment on the kinetics of tetrahydrocannabinol metabolites in mouse brain". Drug Metabolism and Disposition. ج. 23 ع. 8: 825–831. PMID:7493549.
- ^ Klein C، Karanges E، Spiro A، Wong A، Spencer J، Huynh T، Gunasekaran N، Karl T، Long LE، Huang XF، Liu K، Arnold JC، McGregor IS (نوفمبر 2011). "Cannabidiol potentiates Δ⁹-tetrahydrocannabinol (THC) behavioural effects and alters THC pharmacokinetics during acute and chronic treatment in adolescent rats". Psychopharmacology. ج. 218 ع. 2: 443–457. DOI:10.1007/s00213-011-2342-0. PMID:21667074.
- ^ Hunt CA، Jones RT، Herning RI، Bachman J (يونيو 1981). "Evidence that Cannabidiol Does Not Significantly Alter the Pharmacokinetics of Tetrahydrocannabinol in Man". Journal of Pharmacokinetics and Biopharmaceutics. ج. 9 ع. 3: 245–260. DOI:10.1007/BF01059266. PMID:6270295.
- ^ United States Adopted Names Council: Statement on a nonproprietary name نسخة محفوظة 05 يوليو 2013 على موقع واي باك مشين. [وصلة مكسورة]
- ^ "Fact Sheet — Sativex". Health Canada. مؤرشف من الأصل في 2017-04-28. اطلع عليه بتاريخ 2013-05-16.
- ^ "Cannabis-Derived Dravet Syndrome Drug Gets US Orphan Drug Approval". 18 نوفمبر 2013. مؤرشف من الأصل في 2018-06-26. اطلع عليه بتاريخ 2015-07-21.
- ^ Torres, Kristina (September 30, 2015). "Georgia doctors encouraged in study of medical marijuana". The Atlanta Journal. مؤرشف من الأصل في 7 مايو 2016. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Jones PG، Falvello L، Kennard O، Sheldrick GM، Mechoulam R (1977). "Cannabidiol". Acta Crystallogr. B. ج. 33 ع. 10: 3211–3214. DOI:10.1107/S0567740877010577.
- ^ Mechoulam R، Ben-Zvi Z، Gaoni Y (1968). "Hashish—XIII On the nature of the beam test". Tetrahedron. ج. 24 ع. 16: 5615–5624. DOI:10.1016/0040-4020(68)88159-1. PMID:5732891.
- ^ Gaoni Y، Mechoulam R (1966). "Hashish—VII The isomerization of cannabidiol to tetrahydrocannabinols". Tetrahedron. ج. 22 ع. 4: 1481–1488. DOI:10.1016/S0040-4020(01)99446-3.
- ^ Petrzilka T، Haefliger W، Sikemeier C، Ohloff G، Eschenmoser A (1967). "Synthese und Chiralität des (−)-Cannabidiols". Helv. Chim. Acta. ج. 50 ع. 2: 719–723. DOI:10.1002/hlca.19670500235. PMID:5587099.
- ^ Gaoni Y، Mechoulam R (1985). "Boron trifluoride etherate on alumuna — a modified Lewis acid reagent. An improved synthesis of cannabidiol". Tetrahedron Letters. ج. 26 ع. 8: 1083–1086. DOI:10.1016/S0040-4039(00)98518-6.
- ^ Kobayashi Y، Takeuchi A، Wang YG (2006). "Synthesis of cannabidiols via alkenylation of cyclohexenyl monoacetate". Org. Lett. ج. 8 ع. 13: 2699–2702. DOI:10.1021/ol060692h. PMID:16774235.
- ^ Marks MD، Tian L، Wenger JP، Omburo SN، Soto-Fuentes W، He J، Gang DR، Weiblen GD، Dixon RA (2009). "Identification of candidate genes affecting Δ9-tetrahydrocannabinol biosynthesis in Cannabis sativa". Journal of Experimental Botany. ج. 60 ع. 13: 3715–3726. DOI:10.1093/jxb/erp210. PMC:2736886. PMID:19581347.
- ^ Taura, F., Sirikantaramas, S., Shoyama, Y., Yoshikai, K., Shoyama, Y., Morimoto, S. (2007). "Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa". FEBS Letters. ج. 581 ع. 16: 2929–34. DOI:10.1016/j.febslet.2007.05.043. PMID:17544411.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Romney، Lee (13 سبتمبر 2012). "On the frontier of medical pot to treat boy's epilepsy". Los Angeles Times. مؤرشف من الأصل في 2018-10-21.
- ^ Good، Alastair (26 أكتوبر 2010). "Growing marijuana that won't get you high". The Daily Telegraph. London. مؤرشف من الأصل في 2014-11-02.
- ^ Jones, Whitney. "Hemp Oil Not a Source of CBD Which Could Be Used in Epilepsy Treatments" (بالإنجليزية). Archived from the original on 2018-09-23.
- ^ Sachs J، McGlade E، Yurgelun-Todd D (أكتوبر 2015). "Safety and Toxicology of Cannabinoids". Neurotherapeutics. ج. 12 ع. 4: 735–746. DOI:10.1007/s13311-015-0380-8. PMC:4604177. PMID:26269228.
- ^ "Industrial Hemp | Department of Agriculture – Plants". Colorado.gov. مؤرشف من الأصل في 2018-08-26. اطلع عليه بتاريخ 2016-12-04.
- ^ Firger، Jessica (23 أكتوبر 2015). "The Great Kentucky Hemp Experiment". Newsweek.com. مؤرشف من الأصل في 2019-03-10. اطلع عليه بتاريخ 2016-12-04.
- ^ Shear, Michael D. (February 7, 2014) In Signing Farm Bill, Obama Extols Rural Growth. New York Times. نسخة محفوظة 14 نوفمبر 2017 على موقع واي باك مشين.
- ^ Patton، Janet (5 مايو 2015). "Hemp industry is growing in Kentucky, attracting processors, investment | Lexington Herald-Leader". Kentucky.com. مؤرشف من الأصل في 2019-02-24. اطلع عليه بتاريخ 2016-12-04.
- ^ An act relating to authorizing the growing of industrial hemp، No. SSB 5012 of March 23, 2015. اطلع عليه بتاريخ May 1, 2017.
- ^ Engrossed Substitute Senate Bill 6206، March 1, 2016. اطلع عليه بتاريخ May 1, 2017.
- ^ State Industrial Hemp Statutes. U.S. National Conference of State Legislatures (August 19, 2016) نسخة محفوظة 03 أغسطس 2017 على موقع واي باك مشين.
- ^ (PDF) https://web.archive.org/web/20170211042122/http://health.utah.gov/hempregistry/HempExtractNew.pdf. مؤرشف من الأصل (PDF) في 2017-02-11.
{{استشهاد ويب}}: الوسيط|title=غير موجود أو فارغ (مساعدة) - ^ "HB0105". le.utah.gov (بالإنجليزية). Archived from the original on 2018-12-14. Retrieved 2017-05-26.
- ^ "Hemp Registry | Utah Department of Health". health.utah.gov (بالإنجليزية الأمريكية). Archived from the original on 2019-02-09. Retrieved 2017-05-26.
- ^ "Poisons Standard March 2016". Legislation.gov.au. مؤرشف من الأصل في 2017-09-09. اطلع عليه بتاريخ 2016-12-04.
- ^ "Controlled Drugs and Substances Act – Schedule II". Laws-lois.justice.gc.ca. مؤرشف من الأصل في 2019-05-14. اطلع عليه بتاريخ 2016-12-04.
- ^ "CosIng – Cosmetics – GROWTH – European Commission". Ec.europa.eu. مؤرشف من الأصل في 2019-01-13. اطلع عليه بتاريخ 2016-12-04.
- ^ "Food - European Commission". مؤرشف من الأصل في 2019-04-03.
- ^ "Support the EIHA CBD position paper - EIHA European Industrial Hemp Association". مؤرشف من الأصل في 2018-09-30.
- ^ أ ب Fournier، G.؛ Beherec، O.؛ Bertucelli، S. (2003). "Intérêt du rapport Δ-9-THC / CBD dans le contrôle des cultures de chanvre industriel". Annales de Toxicologie Analytique. ج. 15 ع. 4: 250–259. DOI:10.1051/ata/2003003.
- ^ Läkemedelsverket. "LMF - Läkemedelsverket / Medical Products Agency". lakemedelsverket.se (بالسويدية). Archived from the original on 2018-08-26. Retrieved 2017-05-26.
- ^ "Sativex - FASS Allmänhet". www.fass.se (بالسويدية). Archived from the original on 2018-08-26. Retrieved 2017-05-26.
- ^ "Sativex Oromucosal Spray – Summary of Product Characteristics (SPC) – (eMC)". Medicines.org.uk. مؤرشف من الأصل في 2019-03-28. اطلع عليه بتاريخ 2016-12-04.
- ^ "MHRA statement on products containing Cannabidiol (CBD)". Gov.uk. 14 ديسمبر 2016. مؤرشف من الأصل في 2019-05-10.
- ^ "Products containing cannabidiol (CBD) – overview". swissmedic.ch. مؤرشف من الأصل في 2017-04-17. اطلع عليه بتاريخ 2017-05-20.
- ^ "Cannabis à faible teneur en THC et CBD". bag.admin.ch. مؤرشف من الأصل في 2018-06-16. اطلع عليه بتاريخ 2017-05-20.
| في كومنز صور وملفات عن: كانابيديول |