متلازمة لوجان-فرينس
| متلازمة لوجان-فرينس | |
|---|---|
متلازمة لوجان-فرينس في ذكر بالغ صغير، مه وجود بعض الأعراض مثل الوجه الطويل النحيف والذقن المسحوب.
| |
| معلومات عامة | |
| الاختصاص | طب نفسي |
| تعديل مصدري - تعديل | |
متلازمة لوجان-فرينس أو متلازمة لوجان أو التخلف العقلي الوراثي السائد المصحوب بأعراض متلازمة مارفان،[1][2][3] هو مرض وراثي سائد على الكروموسوم X الذي يسبب درجات متفاوتة من التخلف العقلي الطفيف إلى المتوسط وبعض الأعراض الشبيهة بأعراض متلازمة مارفان.[4][5] تشمل هذه الأعراض القامة النحيفة الطويلة، والأطراف الطويلة النحيفة.[5] يصاحب متلازمة لوجان-فرينس اضطرابات أخرى في السلوك وبعض الاضطرابات النفسية، بالإضافة إلى بعض التشوهات الدماغية والقلبية.[6][7][8] تتخذ الصورة الوراثية لمتلازمة لوجان-فرينس النمط السائد، ويُعزى هذا إلى طفرة في جين MED12 على الكروموسوم X.[3]
لا يوجد أي علاج لهذا الخلل الجيني في الوقت الحالي، بينما يظل السبب الريسي لهذا الخلل الجيني مجهولًا حتى وقتنا هذا.[9]
الخصائص[عدل]
تتراوح درجات التخلف العقلي في متلازمة لوجان-فرينس من التخلف العقلي الطفيف إلى المتوسط، كما تم الإبلاغ عن حدوث حالات شديدة الخطورة من التخلف العقلي كذلك.[10][11] يعتبرعدم تخليق الجسم الثفني من أكثر حالات التشوهات الدماغية شهرةً، وهو ما ينتج عنه خلل في التطور الجنيني للجسم الثفني (وهو جزء من تركيب الدماغ في الثدييات يسمح بانتقال الأعصاب بين نصفي الكرة المخية) مما يؤدي إلى عدم تكوينه.[7][12] يمثل التخلف العقلي من بين الأعراض العصبية المصحابة لعدم تخليق الجسم الثفني، 73% من الأعراض.[12] على الرغم من ذلك لم يتم وضع رابطة بين عدم تخليق الجسم الثفني والتخلف العقلي المصاحب لمتلازمة لوجان-فرينس.[13]
الأعراض النفسية[عدل]
عادةً ما تظهر الأعراض النفسية والاضطرابات السلوكية في متلازمة لوجان-فرينس، وهو ما يتم أخذه في الحسبان عند التشخيص.[7] من أكثر تلك الأعراض شيوعًا هو طيف التوحد، لذا تعتبر متلازمة لوجان-فرينس هي أحد الأمراض الجينية المصحوبة بالتوحد.[7][14] كان من بين الاضرابات النفسية والسلوكية الأخرى المتواجدة في متلازمة لوجان-فرينس: الذهان[15] والفصام [16] واضطراب نقص الانتباه مع فرط النشاط[13][17] والعدوان [17] واضطراب التحدي الاعتراضي[13][18] واضطراب الوسواس القهري[13] والخجل وعجز التعلم [13] واضطراب الذاكرة قصيرة الأمد [13] واضطراب القلق الاجتماعي [13] واضطراب الأكل [13] وسوء التغذية والأمراض نفسية المنشأ [13] وفقدان الشهية وهوس الحرائق.[7][13][18]
وبينما يتم توقع حدوث مثل تلك الاضطرابات النفسية والسلوكية في حالات الإصابة بمتلازمة لوجان-فرينس، إلا أنه توجد بعض الحالات التي تتمتع بالحفاظ على القوى العقلية والسلوكية والنفسية الطبيعية، مثل حل المشكلات ومستويات الذكاء والفهم الطبيعيين.[19] عادةً ما يصاب أصحاب متلازمة لوجان-فرينس بمرض الفصام. وحيث أن الفصام يعتبر من أحد الأسباب التي تسبب التخلف العقلي، لذا يجب وضع متلازمة لوجان-فرينس في التشخيص التفريقي للفصام مع إجراء الاختبارات الجينية والنفسية اللازمة.[16]
أشباه مارفان[عدل]
عادةً ما يتم الاعتماد على أعراض متلازمة مارفان لتشخيص حالات لوجان-فرينس وتفرقتها عن الأشكال الأخرى من التخلف العقلي المرتبط بالكروموسوم X.[10]
يصف مصطلح أشباه مارفان بعض الأعراض الطبية الشبيهة بمتلازمة مارفان. تتشارك كلا المتلازمتين بعض الاضطرابات الوراثية الأخرى، أشهرها هو تكون الورم الصماوي المتعدد النوع 2.[20]
تشمل تلك الأعراض الآتي:
- الوجه الطويل النحيف.[5][9]
- القامة الطويلة.[3][9]
- الأطراف والأصابع وأصابع القدم الطويلة النحيفة مع مدى واسع من حركة المفاصل.[3][21][22]
- سلاميات قصيرة لأصابع القدم الكبيرة وطول أصابع القدم الأخرى.
يتأخر تشخيص متلازمة لوجان-فرينس وتفرقتها عن متلازمة مارفان لعدم ظهور العديد من تلك الأعراض حتى سن المراهقة.[2]
الشذوذ القحفي (الوجه والدماغ)[عدل]
تشمل اضطرابات الوجه والدماغ:
- نقص تنسج الفك العلوي (نقص نمو عظام الفك العلوي)[9]
- الفك السفلي الصغير والذقن المسحوبة.[3][17]
- الحنك ذا التقوس العالي مع ازدحام وعدم ترتيب الأسنان العلوية.[5][7]
- ضخامة الرأس[3][9] (تضخم الجمجمة) وبروز الجبهة وخنف الحديث [5][7] وانخفاض مستوى الأذنين.
- الأنف الطويل وضيق منطقة ما فوق الأنف والنثرة القصيرة (النثرة هي المنخفض الذي يعتلي الشفة العلوية أسفل الأنف)
- نقص التوتر العضلي والصدر المقعر[9] وتضخم الخصية الطفيف في الذكور ونوبات الصرع.[9][17]
ينتج خنف الحديث من قصور تكوين الخفاق البلعومي، وهو عيب خلقي في تكوين عاصرة الخفاق البلعومي مما يسمح بمرور كمية كبيرة من الهواء إلى جوف الأنف خلال الحديث.[23][24] يمكن أيضًا إرجاع خنف الحديث في متلازمة لوجان-فرينس إلى فشل شراع الحنك واللهاة في الوصول إلى الجانب الخلفي للبلعوم خلال الحديث، وهذه الحالات عادةً ما يصاحبها حالة مرضية تعرف باسم فلح الشفة والحنك.[13][25]
تشوهات القلب والأوعية الدموية[عدل]
لوحظ العديد من التشوهات القلبية في حالات عديدة مصابة بمتلازمة لوجان-فرينس، أكثرها على الإطلاق كان تمددات شريان الأبهر الصاعد،[26] وتقسم الأبهر الصاعد. يرتبط تمدد الأبهر الصاعد بشكل كبير بتسلخ جدار الأبهر الصاعد، وهو ما ينتج عنه التكيسات الدموية الأبهرية. ونظرًا لتشكيل تلك التشوهات خطرًا على صحة المريض، سرعان ما يتم إجراء تخطيط صدى القلب فور التأكد من تشخيص المتلازمة، جنبًا إلى جنب من إجراء تصوير بالرنين المغناطيسي للدماغ لاحتمالية عدم تخليق الجسم الثفني. كان عيب الحاجز البطيني وعيب الحاجز الأذيني من ضمن التشوهات القلبية الأخرى التي لوحظت في حالات متلازمة لوجان-فرينس.[8][17]
السبب[عدل]
تم اعتبار حدوث طفرة مغلطة في جين MED12 المتواجد على كروموسوم X سببًا رئيسيًأ لمتلازمة لوجان-فرينس.[3][27] الطفرات المغلطة هي طفرات نقطية حيث يتم إدخال الشيفرة الجينية لحمض أميني من المفترض ألا يتواجد على تتابع الأحماض الأمينية لأحد البروتينات بدلًا من الحمض الأميني المفترض تواجده في هذا التتابع عند نقطة معينة. تحدث الطفرة المغلطة في جين MED12 عند النقطة p.N1007S. وهذا يعني أنه تم استبدال الحمض الأميني أسبارجين، والمفترض تواجده عند الموقع 1007 على جين MED12، بالحمض الأميني سيرين.[27] يتسب هذا الخلل الجيني في تخليق خاطيء للبروتينات المسؤول عنها هذا الجين وبالتالي خطأ في وظيفتها، مما يؤدي إلى تلك الاضطرابات.[3][9]
آلية المرض[عدل]

يعتبر جين MED12 أحد الجينات المتحكمة في نسخ الحمض النووي الريبوزي الرسول في الثدييات.[28][29]
يعمل هذا الجين كحلقة وصل بين الانزيم وباقي عوامل النسخ المرتبطة بهذا الحمض. يحتوي مركب النسخ هذا على 30 وحدة فرعية، بينما يلزم وجود بعضًا من تلك الوحدات فقط لاتمام تلك العملية في الخلايا والأنسجة المختلفة.[30] في الوقت الحالي، لا تزال الآلية المحددة لحدوث متلازمة لوجان-فرينس والاضطرابات السلوكية والنفسية اللاحقة بها نتيجةً للخلل الجيني في جين MED12 غير واضحة. تظهر أعراض أشباه مارفان مثل الحنك ذو التقوس العالي الخاصة بمتلازمة لوجان-فرينس في متلازمة مارفان وهو أحد أمرض النسيج الضام. ومما يرجح بقوة مشاركة هذ الخلل الجيني في آلية مرض تلك المتلازمة هو تمددات الأبهر الصاعد الذي يوضح خلل في الجين المسؤول عن أحد الأنسجة الضامة.[1][5][8][13]
حصل العلماء على العديد من النتائج المبهرة في دراسة طفرات جين MED12 في الدانيو المخطط، والذي اتخذه العلماء كنموذج حي للفقاريات.[31][32][33] وجد العلماء أن طفرة جين MED12 في ذلك النوع من الأسماك مسؤولة عن طفرة عدم الحركة، وهو ما صاحبها تشوهات عصبية وقلبية، على الرغم من عدم إصابة جميع الأعصاب. عند إعطاء تلك الأسماك حمض نووي ريبوزي رسول الخاص بجين MED12 استعادت تلك الأسماك صحتها. يعتبر جين MED12 أيضًا أحد الجينات اللازمة لتفعيل جين SOX9 اللازم لنمو الغضاريف والعظام والأعصاب.[34][35][36] كان من ضمن التشوهات الناجمة عن هذا الخلل الجيني في تلك الأسماك هو قصور تكوين العرف العصبي، وهو ما أحدث خللًا في الجهاز العصبي الذاتي والجهاز العصبي المحيطي وتشوهات الخلايا الأم للغضاريف والعظام، وهو ما يماثل عدم تكوين الجسم الثفني وتشوهات الوجه والرأس المرتبطة بالغضاريف والعظام في البشر.[3]
علم الوراثة[عدل]
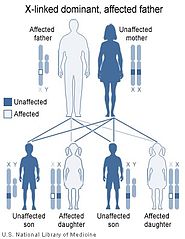
يتم وراثة متلازمة لوجان-فرينس بصورة سائدة على الكروموسوم X.[9][13][37] وهذا يعني أن الخلل الجيني في جين MED12 متواجد على الكروموسوم X، ووجود نسخة من الجين المختل كافي لوراثة هذا الخلل الجيني من أحد الأبوين. يتمتع الذكور باقترانية زيجوتية للكروموسوم X الذي يمتلكون منه نسخة واحدة. وبالتالي تشيع تلك الحالات بين الذكور أكثر من الإناث.[13][37]
وحيث أن الكروموسوم X هو أحد كروموسومات تحديد الجنس (والآخر هو الكروموسوم Y) ترتبط الصفات الوراثية المنتقلة من خلال الكروموسوم X بجنس الأب الحامل للخل الجيني. يرجع هذا إلى امتلاك الإناث لزوجين من كروموسومات X، بينما يمتلك الذكور نسخةً واحدةً منه. كما يلعب الفرق بين الوراثة السائدة والمتنحية دورًا هامًا في تحديد انتقال الصفات الوراثية من جيل الآباء إلى جيل الأبناء.
في حالات الوراثة السائدة المرتبطة بالكروموسوم X يصبح كلًا من الذكور والإناث معرضان لخطر الإصابة (مع وجود احتمالية إصابة الذكور أعلى من الإناث). يحدث عكس هذا في الوراثة المتنحية المرتبطة بالكروموسوم X، إذ ترتفع نسبة إصابة الإناث عن الذكور لتمتعهم بالافترانية الزيجوتية في تلك الحالة.[13][37]
كما تم الإبلاغ أيضًا عن بعض الحالات التي حدثت بها متلازمة لوجان-فرينس في بعض الذكور دون أن يكون لديهم تاريخ مرضي عائلي بحدوث حالات مشابهة لمتلازمة لوجان-فرينس.[13][15][38]
التشابه بين المتلازمة والأمراض الوراثية الأخرى[عدل]
وُجدت بعض الحالات المشابهة في التخلف العقلي والأعراض الأخرى لمتلازمة لوجان-فرينس في حالة حدوث حذف في التيلوميرات الفرعية على الموقع الكروموسومي في الكروموسوم 5. صاحب الحذف الجيني في تلك المنطقة في الكروموسوم 5 أعراض مثل التخلف العقلي والاضطرابات النفسية والسلوكية والتوحد وضخامة الرأس وخنف الحديث، بالإضافة إلى متلازمة المواء.[25][39] اقترح فرينس عام 2006 ضرورة إجراء اختبار تفصيلي للكروموسوم 5 باستخدام التهجين الموضعي المتألق للتشخيص التفريقي بينه وبين متلازمة لوجان-فرينس.[9]
كما وجد أن طفرة جين UPF3B على الكروموسوم X ترتبط بالتخلف العقلي.[40] يعتبر جين UPF3B أحد مكونات مركب تحليل الحمض النووي الريبوزي الرسول المسؤول عن مراقبة طفرات ذلك الحمض النووي.ينتج عن الطفرة في ذلك الجين خلل في تلك العملية مما ينتج شرائط قصيرة من الحمض النووي الريبوزي الرسولوما يتبعه من تخليق بروتينات مختلة الوظيفة وما يلحق بها من خلل في النمو البدني والعقلي.[41] تم العثور على أشخاص مصابين بمتلازمة لوجان-فرينس من عائلتين مختلفتين لديهم خلل في جين UPF3B، وهو ما يثبت أن بإمكان تلك المتلازمات الجينية أن تتداخل.[42]
التشخيص[عدل]
على الرغم من اعتماد تشخيص متلازمة لوجان-فرينس على وجود التخلف العقلي وأعراض أشباه مارفان في المرضى، إلا أنه لا يتم تأكيد التشخيص إلا من خلال إجراء اختبار لتحديد وجود طفرة مغلطة في الموقع p.N1007S في جين MED12.[3][9][10]
التشخيص التفريقي[عدل]
في التشخيص التفريقي لمتلازمة لوجان-فررينس، تتشابه متلازمة أوبيتز-كافيجيا مع أعراض لوجان-فرينس بالإضافة إلى وجود طفرة مغلطة في جين MED12. من ضمن الأعراض المتشابهة بين المتلازمتين: التخلف العقلي المنتققل عبر الكروموسوم X، فرط النشاط، ضخامة الرأس، عدم تخليق الجسم الثفني، وقلة التوتر العضلي. بينما تتفرد متلازمة أوبيتز-كافيجا بفرط التحدث، فرط القوة في الأنشطة الاجتماعية، رتق الشرج (انغلاق فتحة الشرج) وفرط تباعد العينين.[43][44]
في حين تتصف متلازمة لوجان-فرينس بوجود طفرة مغلطة في الموقع p.N1007S في جين MED12، تتصف متلازمة أوبيتز-كافيجيا بوجود طفرة مغلطة في الموقع p.R961W في جين MED12.[3][9][13][45]
العلاج[عدل]
بينما لا يوجد علاج محدد للسبب الوراثي الأساسي لمتلازمة لوجان-فرينس، يمكن أخذ الإجراءات التصحيحية والتدابير الوقائية والتدخلات العلاجية لعلاج مشاكل الوجه والرأس والعظام والاضطرابات النفسية في الاعتبار. كما يجب إجرا التدابير الازمة لمراقبة وعلاج المضاعفات الأكثر خطورة مثل نوبات الصرع والتشوهات القلبية. بالإضافة إلى ذلك، يفضل ينبغي أن يولي الأطباء اهتمام وثيق ورعاية ومتابعة متخصصة لتشخيص ومنع حدوث الاضطرابات النفسية والسلوكية المصاحبة مثل الذهان أو العدوان.[9]
الاحصاءات الوبائية[عدل]
متلازمة لوجان-فرينس هي مرض وراثي سائد ينتقل عبر الكروموسوم X، وبالتالي يشيع بين الذكور عن الإناث. لم يتم إحصاء نسبة حدوث تلك الحالات بين السكان بشكل دقيق حتى الآن.[9]
التاريخ[عدل]
سُميت تلك المتلازمة بذلك الاسم وفقًا للطبيبين جون إنريك لوجان وجون بيير فرينس.[21] تم وصف التخلف العقلي والأعراض الشبيهة بمتلازمة مارفان وتشوهات الرأس والدماغ مثل الحنك ذا التقوس العالي بواسطة لوجان وآخرون عام 1984.[17] أجري هذا البحث على أربعة أفراد ذكور في هائلة واحدة تجمعهم قرابة العصب.[3][13][17] كما تم وصف نفس الأعراض في عائلات أخرى، بما في ذلك أخوين، بواسطة فرينس وآخرون في أوائل عام 1987. ومن ثم سميت تلك المتلازمة بمتلازمة لوجان-فرينس.[37]
انظر أيضًا[عدل]
مراجع[عدل]
- ^ أ ب Lacombe، D.؛ Bonneau، D.؛ Verloes، A.؛ Couet، D.؛ Koulischer، L.؛ Battin، J. (1993). "Lujan-Fryns syndrome (X-linked mental retardation with marfanoid habitus): report of three cases and review". Genetic counseling (Geneva, Switzerland). ج. 4 ع. 3: 193–198. ISSN:1015-8146. PMID:8267926.
- ^ أ ب Fryns، J. P.؛ Van Den Berghe، H. (1991). "X-linked mental retardation with Marfanoid habitus: a changing phenotype with age?". Genetic counseling (Geneva, Switzerland). ج. 2 ع. 4: 241–244. ISSN:1015-8146. PMID:1799424.
- ^ أ ب ت ث ج ح خ د ذ ر ز س Schwartz، C. E.؛ Tarpey، P. S.؛ Lubs، H. A.؛ Verloes، A.؛ May، M. M.؛ Risheg، H.؛ Friez، M. J.؛ Futreal، P. A.؛ Edkins، S.؛ Teague، J.؛ Briault، S.؛ Skinner، C.؛ Bauer-Carlin، A.؛ Simensen، R. J.؛ Joseph، S. M.؛ Jones، J. R.؛ Gecz، J.؛ Stratton، M. R.؛ Raymond، F. L.؛ Stevenson، R. E. (يوليو 2007). "The original Lujan syndrome family has a novel missense mutation (p.N1007S) in the MED12 gene". Journal of Medical Genetics. ج. 44 ع. 7: 472–477. DOI:10.1136/jmg.2006.048637. ISSN:0022-2593. PMC:2597996. PMID:17369503.
- ^ الوراثة المندلية البشرية عبر الإنترنت (OMIM): 154700
- ^ أ ب ت ث ج ح Fryns، J. P.؛ Buttiens، M.؛ Opitz، J. M.؛ Reynolds، J. F. (أكتوبر 1987). "X-linked mental retardation with marfanoid habitus". American Journal of Medical Genetics. ج. 28 ع. 2: 267–274. DOI:10.1002/ajmg.1320280202. ISSN:0148-7299. PMID:3322000.
- ^ Alonso، P.؛ Pintos، G.؛ Almazan، F.؛ Hernández، L.؛ Loran، E.؛ Menchon، J. M.؛ Vallejo، J. (يوليو 2006). "Eating disorder in a patient with phenotypical features of Lujan-Fryns syndrome". Clinical Dysmorphology. ج. 15 ع. 3: 181–184. DOI:10.1097/01.mcd.0000220610.24908.a4. ISSN:0962-8827. PMID:16760741.
- ^ أ ب ت ث ج ح خ Lerma‐Carrillo، I.؛ Molina، J. D.؛ Cuevas-Duran، T.؛ Julve-Correcher، C.؛ Espejo-Saavedra، J. M.؛ Andrade-Rosa، C.؛ Lopez-Muñoz، F. (ديسمبر 2006). "Psychopathology in the Lujan-Fryns syndrome: report of two patients and review". American Journal of Medical Genetics Part A. ج. 140 ع. 24: 2807–2811. DOI:10.1002/ajmg.a.31503. ISSN:1552-4825. PMID:17036352.
- ^ أ ب ت Wittine، L. M.؛ Josephson، K. D.؛ Williams، M. S. (أكتوبر 1999). "Aortic root dilation in apparent Lujan-Fryns syndrome". American Journal of Medical Genetics. ج. 86 ع. 5: 405–409. DOI:10.1002/(SICI)1096-8628(19991029)86:5<405::AID-AJMG2>3.0.CO;2-1. ISSN:0148-7299. PMID:10508979.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص Buggenhout، G. V.؛ Fryns، J. -P. (يوليو 2006). "Lujan-Fryns syndrome (mental retardation, X-linked, marfanoid habitus)". Orphanet Journal of Rare Diseases (Free full text). ج. 1: 26. DOI:10.1186/1750-1172-1-26. PMC:1538574. PMID:16831221.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ أ ب ت Fryns، J. P.؛ Buttiens، M.؛ Van Den Berghe، H. (يناير 1988). "Chromosome X-linked mental retardation and marfanoid syndrome". Journal de Genetique Humaine. ج. 36 ع. 1–2: 123–128. ISSN:0021-7743. PMID:3379374.
- ^ Mégarbané A، C. C.؛ Chammas، C. (1997). "Severe mental retardation with marfanoid habitus in a young Lebanese male. A diagnostic challenge". Genetic Counseling (Geneva, Switzerland). ج. 8 ع. 3: 195–200. ISSN:1015-8146. PMID:9327261.
- ^ أ ب Jeret، J. S.؛ Serur، D.؛ Wisniewski، K. E.؛ Lubin، R. A. (1987). "Clinicopathological findings associated with agenesis of the corpus callosum". Brain & Development. ج. 9 ع. 3: 255–264. DOI:10.1016/s0387-7604(87)80042-6. ISSN:0387-7604. PMID:3310713.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع الوراثة المندلية البشرية عبر الإنترنت (OMIM): 309520
- ^ Artigas-Pallarés، J.؛ Gabau-Vila، E.؛ Guitart-Feliubadaló، M. (يناير 2005). "Syndromic autism: II. Genetic syndromes associated with autism". Revista de Neurologia. 40 Suppl 1: S151–S162. ISSN:0210-0010. PMID:15736079.
- ^ أ ب Lalatta، F.؛ Livini، E.؛ Selicorni، A.؛ Briscioli، V.؛ Vita، A.؛ Lugo، F.؛ Zollino، M.؛ Gurrieri، F.؛ Neri، G. (فبراير 1991). "X-linked mental retardation with marfanoid habitus: first report of four Italian patients". American Journal of Medical Genetics. ج. 38 ع. 2–3: 228–232. DOI:10.1002/ajmg.1320380211. ISSN:0148-7299. PMID:2018063.
- ^ أ ب De Hert، M.؛ Steemans، D.؛ Theys، P.؛ Fryns، J. P.؛ Peuskens، J. (أبريل 1996). "Lujan-Fryns syndrome in the differential diagnosis of schizophrenia". American Journal of Medical Genetics. ج. 67 ع. 2: 212–213. DOI:10.1002/(SICI)1096-8628(19960409)67:2<212::AID-AJMG13>3.0.CO;2-M. PMID:8723050.
- ^ أ ب ت ث ج ح خ Lujan، J. E.؛ Carlin، M. E.؛ Lubs، H. A.؛ Opitz، J. M. (يناير 1984). "A form of X-linked mental retardation with marfanoid habitus". American Journal of Medical Genetics. ج. 17 ع. 1: 311–322. DOI:10.1002/ajmg.1320170124. ISSN:0148-7299. PMID:6711603.
- ^ أ ب Williams، M. S. (ديسمبر 2006). "Neuropsychological evaluation in Lujan-Fryns syndrome: commentary and clinical report". American Journal of Medical Genetics Part A. ج. 140 ع. 24: 2812–2815. DOI:10.1002/ajmg.a.31501. ISSN:1552-4825. PMID:17103446.
- ^ Donders، J.؛ Toriello، H.؛ Van Doornik، S. (يناير 2002). "Preserved neurobehavioral abilities in Lujan-Fryns syndrome". American Journal of Medical Genetics. ج. 107 ع. 3: 243–246. DOI:10.1002/ajmg.10144. ISSN:0148-7299. PMID:11807907.
- ^ Prabhu، M.؛ Khouzam، R. N.؛ Insel، J. (نوفمبر 2004). "Multiple endocrine neoplasia type 2 syndrome presenting with bowel obstruction caused by intestinal neuroma: case report". Southern Medical Journal. ج. 97 ع. 11: 1130–1132. DOI:10.1097/01.SMJ.0000140873.29381.12. ISSN:0038-4348. PMID:15586612.
- ^ أ ب synd/3838 على قاموس من سمى هذا؟
- ^ Buntinx، I. M.؛ Willems، P. J.؛ Spitaels، S. E.؛ Van Reempst، P. J.؛ De Paepe، A. M.؛ Dumon، J. E. (أبريل 1991). "Neonatal Marfan syndrome with congenital arachnodactyly, flexion contractures, and severe cardiac valve insufficiency". Journal of Medical Genetics. ج. 28 ع. 4: 267–273. DOI:10.1136/jmg.28.4.267. ISSN:0022-2593. PMC:1016831. PMID:1856834.
- ^ Willging، J. P. (أكتوبر 1999). "Velopharyngeal insufficiency". International Journal of Pediatric Otorhinolaryngology. 49 Suppl 1: S307–S309. DOI:10.1016/S0165-5876(99)00182-2. ISSN:0165-5876. PMID:10577827.
- ^ Warren، D. W.؛ Dalston، R. M.؛ Mayo، R. (يوليو 1994). "Hypernasality and velopharyngeal impairment". The Cleft Palate-Craniofacial Journal. ج. 31 ع. 4: 257–262. DOI:10.1597/1545-1569(1994)031<0257:HAVI>2.3.CO;2. ISSN:1055-6656. PMID:7918520.
- ^ أ ب Stathopulu، E.؛ Ogilvie، C. M.؛ Flinter، F. A. (يونيو 2003). "Terminal deletion of chromosome 5p in a patient with phenotypical features of Lujan-Fryns syndrome". American Journal of Medical Genetics Part A. ج. 119A ع. 3: 363–366. DOI:10.1002/ajmg.a.10268. ISSN:1552-4825. PMID:12784307.
- ^ Gambarin، F.؛ Favalli، V.؛ Serio، A.؛ Regazzi، M.؛ Pasotti، M.؛ Klersy، C.؛ Dore، R.؛ Mannarino، S.؛ Viganò، M.؛ Odero، A.؛ Amato، S.؛ Tavazzi، L.؛ Arbustini، E. (أبريل 2009). "Rationale and design of a trial evaluating the effects of losartan vs. Nebivolol vs. The association of both on the progression of aortic root dilation in Marfan syndrome with FBN1 gene mutations". Journal of Cardiovascular Medicine (Hagerstown, Md.). ج. 10 ع. 4: 354–362. DOI:10.2459/JCM.0b013e3283232a45. ISSN:1558-2027. PMID:19430350.
- ^ أ ب الوراثة المندلية البشرية عبر الإنترنت (OMIM): 300188
- ^ Biddick، R.؛ Young، E. (سبتمبر 2005). "Yeast mediator and its role in transcriptional regulation". Comptes rendus biologies. ج. 328 ع. 9: 773–782. DOI:10.1016/j.crvi.2005.03.004. ISSN:1631-0691. PMID:16168358.
- ^ Sims، R. J. 3rd؛ Mandal، S. S.؛ Reinberg، D. (يونيو 2004). "Recent highlights of RNA-polymerase-II-mediated transcription". Current opinion in cell biology. ج. 16 ع. 3: 263–271. DOI:10.1016/j.ceb.2004.04.004. ISSN:0955-0674. PMID:15145350.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء عددية: قائمة المؤلفين (link) - ^ Malik، S.؛ Roeder، R. G. (يونيو 2000). "Transcriptional regulation through Mediator-like coactivators in yeast and metazoan cells". Trends in Biochemical Sciences. ج. 25 ع. 6: 277–283. DOI:10.1016/S0968-0004(00)01596-6. ISSN:0968-0004. PMID:10838567.
- ^ Chakraborty C، H. C.؛ Hsu، C. H.؛ Wen، Z. H.؛ Lin، C. S.؛ Agoramoorthy، G. (فبراير 2009). "Zebrafish: a complete animal model for in vivo drug discovery and development". Current Drug Metabolism. ج. 10 ع. 2: 116–124. DOI:10.2174/138920009787522197. ISSN:1389-2002. PMID:19275547.
- ^ Kari، G.؛ Rodeck، U.؛ Dicker، A. P. (يوليو 2007). "Zebrafish: an emerging model system for human disease and drug discovery". Clinical Pharmacology and Therapeutics. ج. 82 ع. 1: 70–80. DOI:10.1038/sj.clpt.6100223. ISSN:0009-9236. PMID:17495877.
- ^ McGonnell، I. M.؛ Fowkes، R. C. (يونيو 2006). "Fishing for gene function--endocrine modelling in the zebrafish". The Journal of Endocrinology. ج. 189 ع. 3: 425–439. DOI:10.1677/joe.1.06683. ISSN:0022-0795. PMID:16731775. مؤرشف من الأصل (Free full text) في 2019-12-15.
- ^ Wang، X.؛ Yang، N.؛ Uno، E.؛ Roeder، R. G.؛ Guo، S. (نوفمبر 2006). "A subunit of the mediator complex regulates vertebrate neuronal development". Proceedings of the National Academy of Sciences of the United States of America (Free full text). ج. 103 ع. 46: 17284–17289. Bibcode:2006PNAS..10317284W. DOI:10.1073/pnas.0605414103. ISSN:0027-8424. PMC:1859923. PMID:17088561.
- ^ Rau، M. J.؛ Fischer، S.؛ Neumann، C. J. (أغسطس 2006). "Zebrafish Trap230/Med12 is required as a coactivator for Sox9-dependent neural crest, cartilage and ear development". Developmental Biology. ج. 296 ع. 1: 83–93. DOI:10.1016/j.ydbio.2006.04.437. ISSN:0012-1606. PMID:16712834.
- ^ Hong، S. -K.؛ Haldin، C. E.؛ Lawson، N. D.؛ Weinstein، B. M.؛ Dawid، I. B.؛ Hukriede، N. A. (ديسمبر 2005). "The zebrafish kohtalo/trap230 gene is required for the development of the brain, neural crest, and pronephric kidney". Proceedings of the National Academy of Sciences of the United States of America. ج. 102 ع. 51: 18473–18478. Bibcode:2005PNAS..10218473H. DOI:10.1073/pnas.0509457102. ISSN:0027-8424. PMC:1311743. PMID:16344459. مؤرشف من الأصل (Free full text) في 2019-12-15.
- ^ أ ب ت ث Gurrieri، F.؛ Neri، G. (فبراير 1991). "A girl with the Lujan-Fryns syndrome". American Journal of Medical Genetics. ج. 38 ع. 2–3: 290–291. DOI:10.1002/ajmg.1320380225. ISSN:0148-7299. PMID:2018074.
- ^ Fryns، J. P. (فبراير 1991). "X-linked mental retardation with marfanoid habitus". American Journal of Medical Genetics. ج. 38 ع. 2–3: 233–233. DOI:10.1002/ajmg.1320380212. ISSN:0148-7299. PMID:2018064.
- ^ Fang، J. S.؛ Lee، K. F.؛ Huang، C. T.؛ Syu، C. L.؛ Yang، K. J.؛ Wang، L. H.؛ Liao، D. L.؛ Chen، C. H. (يونيو 2008). "Cytogenetic and molecular characterization of a three-generation family with chromosome 5p terminal deletion". Clinical Genetics. ج. 73 ع. 6: 585–590. DOI:10.1111/j.1399-0004.2008.00995.x. ISSN:0009-9163. PMID:18400035.
- ^ الوراثة المندلية البشرية عبر الإنترنت (OMIM): 300298
- ^ Chang، Y. F.؛ Imam، J. S.؛ Wilkinson، M. F. (2007). "The nonsense-mediated decay RNA surveillance pathway". Annual Review of Biochemistry. ج. 76: 51–74. DOI:10.1146/annurev.biochem.76.050106.093909. ISSN:0066-4154. PMID:17352659.
- ^ Tarpey، P. S.؛ Raymond، F. L.؛ Nguyen، L. S.؛ Rodriguez، J.؛ Hackett، A.؛ Vandeleur، L.؛ Smith، R.؛ Shoubridge، C.؛ Edkins، S.؛ Stevens، C.؛ O'Meara، S.؛ Tofts، C.؛ Barthorpe، S.؛ Buck، G.؛ Cole، J.؛ Halliday، K.؛ Hills، K.؛ Jones، D.؛ Mironenko، T.؛ Perry، J.؛ Varian، J.؛ West، S.؛ Widaa، S.؛ Teague، J.؛ Dicks، E.؛ Butler، A.؛ Menzies، A.؛ Richardson، D.؛ Jenkinson، A.؛ Shepherd، R. (سبتمبر 2007). "Mutations in UPF3B, a member of the nonsense-mediated mRNA decay complex, cause syndromic and nonsyndromic mental retardation". Nature Genetics (Free full text). ج. 39 ع. 9: 1127–1133. DOI:10.1038/ng2100. ISSN:1061-4036. PMC:2872770. PMID:17704778.
- ^ Graham، J. M.؛ Superneau، D.؛ Rogers، R. C.؛ Corning، K.؛ Schwartz، C. E.؛ Dykens، E. M. (1999). "Clinical and behavioral characteristics in FG syndrome". American Journal of Medical Genetics. ج. 85 ع. 5: 470–475. DOI:10.1002/(SICI)1096-8628(19990827)85:5<470::AID-AJMG7>3.0.CO;2-S. PMID:10405444.
- ^ Jr، G.؛ Visootsak، M.؛ Dykens، J.؛ Huddleston، E.؛ Clark، L.؛ Jones، R. D.؛ Moeschler، K. L.؛ Opitz، J. B.؛ Morford، J. M.؛ Simensen، R.؛ Rogers، R. C.؛ Schwartz، C. E.؛ Friez، M. J.؛ Stevenson، R. E. (ديسمبر 2008). "Behavior of 10 patients with FG Syndrome (Opitz-Kaveggia Syndrome) and the p.R961W Mutation in the MED12 Gene". American Journal of Medical Genetics Part A. ج. 146A ع. 23: 3011–3017. DOI:10.1002/ajmg.a.32553. ISSN:1552-4825. PMC:3092600. PMID:18973276.
- ^ الوراثة المندلية البشرية عبر الإنترنت (OMIM): 305450
مصادر خارجية[عدل]
- GeneReview/NIH/UW entry on MED12-Related Disorders
- Van Buggenhout, G. J. C. M.; Trommelen, J. C. M.; Brunner, H. G.; Hamel, B. C. J.; Fryns, J. P. (Jan 2001). "The clinical phenotype in institutionalised adult males with X-linked mental retardation (XLMR)". Annales de Génétique. 44 (1): 47–55. doi:10.1016/S0003-3995(01)01038-3. ISSN 0003-3995. PMID 11334618.
| في كومنز صور وملفات عن: متلازمة لوجان-فرينس |