تخدير
| تخدير | |
|---|---|
طفل تحت التخدير
| |
| معلومات عامة | |
| من أنواع | وعي متغير |
| التاريخ | |
| وصفها المصدر | موسوعة بلوتو ، وقاموس بروكهاوس وإفرون الموسوعي، والموسوعة السوفيتية الكبرى ، وقاموس بروكهاوس وإفرون الموسوعي، وقاموس بروكهاوس وإفرون الموسوعي الصغير ، والموسوعة البريطانية نسخة سنة 1911، والمرجع الجديد للطلاب ، والموسوعة السوفيتية الأرمينية، المجلد الأول |
| تعديل مصدري - تعديل | |
التخدير هي عملية استخدام الأدوية القادرة على محاصرة الإحساس بالألم بصورة أساسية، وبعض الاحاسيس الأخرى في مجال الطب (خاصة الجراحة، وطب الأسنان). ويشمل: المسكنات (التي تخفف، أو تمنع الألم)، والشلل المؤقت لعضلات الجسم (ارتخاء العضلات)، وفقدان الذاكرة، وفقدان الوعي المؤقت. ويشار للمريض الذي يكون تحت تأثير الأدوية المخدرة بأنه مُخَدَّر.
يّستعمل التخدير لمساعدة المريض على الخضوع للإجراءات الطبية، والعمليات الجراحية دون ألم أو معاناة. ويوجد ثلاثة أسس للتخدير:
- تخدير عام (General Anesthesia): يثبط نشاط الجهاز العصبي المركزي، مما يؤدي إلى فقدان الوعي، وفقدان عام للإحساس يشمل كامل الجسم.
- تهدئة (Sedation): تثبط الجهاز العصبي المركزي إلى أقل درجة، وتثبط القلق وخلق ذاكرة طويلة المدى للأحداث، ولكن دون فقد الوعي.
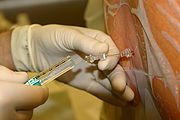
- تخدير ناحي، وتخدير موضعي (Regional Anesthesia): لمنع انتقال النبضات العصبية بين جزء معين من الجسم والجهاز العصبي المركزي، مما يسبب فقد الأحساس في هذا الجزء من الجسم. ويتميز هذا النوع بأن المريض يكون واعِ إلا إذا تم إعطائه مخدر عام، أو مهدئ في نفس الوقت. ويوجد منه نوعان:
- إحصار عصبي طرفي (Peripheral nerve block)، يثبط الإحساس في مكان ما في الجسم، مثل: تخدير الأسنان في مجال طب الأسنان، أو إحصار عصب لتثبيط الإحساس في الطرف بالكامل.
- إحصار عصبي مركزي (Central nerve block)، حيث يتم تخدير منطقة معينة في الجهاز العصبي المركزي نفسه لتثبيط استقبال الإحساس القادم إليه من المناطق الموجودة خارج مكان الإحصار مثل تخدير فوق الجافية، والتخدير النصفي.
ولتجهيز إجراء طبي يقوم طبيب التخدير باختيار وتحديد الجرعات اللازمة من دواء واحد أو أكثر، للوصول إلى نوع ودرجة التخدير المناسبة لنوع الإجراء الطبي، وللمريض. وتشمل أنواع هذه الأدوية: المخدر العام، والمنومات، والمهدئات، والناركوتيات، والمسكنات.
يوجد للتخدير مخاطر رئيسية، ومخاطر ثانوية. ومن أمثلة المخاطر الرئيسية: الوفاة، والنوبة القلبية، والانصمام الرئوي، بينما تشمل المخاطر الثانوية: قيء، وغثيان بعد العملية، وإعادة حجز المريض في المستشفى. ويتناسب حدوث المضاعفات مع حالة المريض الصحية، ودرجة تعقيد العملية الجراحية، ونوع التخدير. غالبا ما يستيقظ المريض خلال دقائق بعد انتهاء تأثير المخدر، ويستعيد قدرته على الإحساس خلال ساعات. ولكن يوجد إستثناء واحد وهو حالة تسمى هذيان ما بعد العملية تتميز باستمرار التشوش، والارتباك لأسابيع، أو شهور بعد العملية، وهي حالة شائعة مع المرضى الذين يخضعون لجراحات القلب، وكبار السن.
استخدامات طبية[عدل]
ينقسم الهدف من التخدير إلى ثلاثة أهداف أساسية:[1]:236
- التنويم (فقدان مؤقت للوعي مع فقدان الذاكرة).
- تسكين الألم (حيث تقلل من الإحساس، وتصد الانعكاسات الذاتية).
- إرتخاء العضلات.
تؤثر أنواع التخدير المختلفة على النتائج النهائية بشكل مختلف، على سبيل المثال: يعمل التخدير الموضعي على تسكين الألم، ويعتبر بنزوديازيبين (يستخدم في التخدير الجزئي) مهدئ يساعد على فقدان الذاكرة، بينما يؤثر التخدير العام على جميع النتائج. ويهدف التخدير إلى الوصول للنتائج المطلوبة التي تناسب الإجراء الجراحي الذي سيخضع له المريض مع تقليل المخاطر التي يمكن أن يتعرض لها إلى أقصى درجة.
ولتحقيق أهداف التخدير، تعمل الأدوية على أجزاء مختلفة، ولكنها متصلة فيما بينها من الجهاز العصبي. على سبيل المثال، ينتج التنويم من عمل الأدوية على أنوية المخ بما يشبه تنشيط النوم، مما يجعل المريض أقل وعيا، وأقل رد فعل للمؤثرات الضارة.[1]:245
بينما يتم إنشاء فقدان الذاكرة بفعل الأدوية على عدة مناطق (متخصصة) في المخ. وبما أن الذاكرة تتحدد قوتها بقوة الروابط بين خلايا عصبية تسمى لدونة مشبكية.[1]:246 فإن كل نوع تخدير ينتج فقدان ذاكرة عن طريق تأثيرات خاصة على تكوين الذاكرة بجرعات مختلفة. حيث يسبب التخدير بالإستنشاق فقدان للذاكرة عن طريق تثبيط عام لأنوية المخ بجرعات أقل من الجرعات المطلوبة لفقد الوعي. ودواء مثل ميدازولام يسبب فقدان للذاكرة خلال مسارات مختلفة عن طريق منع تكوين الذكريات طويلة المدى.[1]:249
مفهوم الوعي هو الرابط بين فقدان الذاكرة والتنويم، فالوعي هو عملية عُليا لتصنيع المعلومات، على سبيل المثال: كلمة «الشمس» تستحضر مشاعر، وذكريات، وإحساس بالدفء أكثر من كونها كرة ساخنة، برتقالية، مستديرة في السماء، وجزء من دورة على مدار 24 ساعة. بالمثل، يمكن للشخص أن يحلم أثناء التخدير، أو يكون لديه وعي بالإجراء الذي يتم وهو تحت التخدير. ويقدّر أن 22% من الناس يحلمون أثناء التخدير العام، وأن حالة واحدة أو اثنين من كل 100 حالة يكون لديهم بعض الوعي يسمى «الوعي أثناء التخدير العام».[1]:253
تقنيات[عدل]
التخدير ليس وسيلة مباشرة للعلاج، ولكنه يسمح للآخرين بالقيام بأشياء لعلاج، أو تشخيص، أو شفاء مرض يمكن أن يكون مؤلم أو له مضاعفات. وأفضل مخدر هو المخدر الذي يحقق النتيجة المطلوبة لإتمام الإجراء الطبي كاملا، مع أقل درجة من المخاطر على المريض. المرحلة الأولى للتخدير هي التي يتم فيها تقييم نسبة الخطر قبل العملية عن طريق معرفة التاريخ المرضي، وفحص الجسم، والاختبارات المعملية. ويسمح تشخيص الحالة البدنية للمريض قبل العملية للطبيب بتقليل مخاطر التخدير. حيث يحقق التاريخ المرضي الكامل الجيد 56% من التشخيص الصحيح، وتزداد النسبة إلى 73% بعد الفحص البدني، وتساعد الاختبارات المعملية في التشخيص ولكن في 3% فقط من الحالات، مما يؤكد ضرورة معرفة التاريخ المرضي الكامل، والفحص البدني قبل التخدير. وتعتبر التقييمات والتجهيزات الخاطئة قبل العملية هي السبب الأساسي في 11% من النتائج السلبية للتخدير.[1]:1003
| التصنيف | الحالة البدنية |
|---|---|
| ASA 1 | شخص سليم |
| ASA 2 | مرض شامل بسيط |
| ASA 3 | مرض شامل شديد |
| ASA 4 | مرض شامل شديد يهدد استمرار الحياة |
| ASA 5 | شخص يحتضر، ولا يتوقع له الحياة دون تدخل جراحي |
| ASA 6 | شخص تم إعلان وفاته بالسكتة الدماغية، وإزالة أعضائه للتبرع بها لشخص آخر |
| E | أضيفت للمرضى الذين يخضعون للإجراءات الطبية الطارئة |
يعتمد جزء من تقييم المخاطر على صحة المريض. ولقد طورت الجمعية الأمريكية لأطباء التخدير مقياس لتقييم الحالة البدنية قبل العملية يسمى «نظام تصنيف الحالة البدنية التابع للجمعية الأمريكية لأطباء التخدير».
يهدف التاريخ المرضي المفصّل قبل العملية إلى اكتشاف الأمراض الجينية (مثل: فرط الحرارة الخبيث، أو نقص الكولين استراز)، والعادات (مثل: التدخين، والإدمان، وشرب الكحوليات)، والصفات البدنية (مثل: السمنة، وصعوبة التنفس)، وأي مرض موجود (خاصة الأمراض التنفسية، وأمراض القلب) يمكن أن يؤثر على التخدير. ويساعد الفحص البدني على تقييم تأثير أي شيء يتم اكتشافه خلال التاريخ المرضي على التخدير، إلى جانب الاختبارات المعملية.[1]:1003–1009
وبصرف النظر عن عموميات تقييم صحة المريض، يجب وضع تقييم بعض العوامل الخاصة التي ترتبط بالجراحة في الاعتبار عند التخدير. على سبيل المثال: عند تخدير الأم أثناء الولادة يجب وضع الطفل في الاعتبار أيضا، وليس الأم فقط. كما تخلق الأورام الخبيثة، والأورام الموجودة في الرئتين أو الحلق تحديا خاصا أثناء التخدير العام. وبعد تحديد صحة المريض الخاضع للتخدير، والنتائج المطلوب الموصول إليها لإتمام إجراء الجراحة، يمكن تحديد نوع المخدر. ويهدف اختيار طريقة الجراحة، وتقنية التخدير إلى تقليل المضاعفات، وتقليل الوقت اللازم للاستفاقة، وتقليل الاستجابة للضغط والتوتر الناتجان من الجراحة.
تخدير عام[عدل]

التخدير هو الحالة التي يتم الوصول إليها عن طريق تأثير الأدوية على مناطق مختلفة، ولكن متصلة فيما بينها في الجهاز العصبي المركزي. وللتخدير العام ثلاثة أهداف (على عكس التخدير الموضعي، أو المهدئات): عدم القدرة على الحركة (شلل مؤقت)، وفقد الوعي، وصد الاستجابة للضغط والتوتر. في أوائل استخدام التخدير، كان يستطيع التخدير تحقيق أول هدفين مما يسمح للجراح بالقيام بالإجراءات اللازمة، ولكن مات الكثير من المرضى بسبب التغييرات الحادة التي حدثت في ضغط الدم، والنبض الناتجة من اعتداءات جراحية ضارة تضع الجسم تحت ضغط. وأخيرا تم التعرف على طريقة صد الاستجابة للضغط الجراحي بواسطة هارفي كوشينغ الذي قام بحقن مخدر موضعي قبل علاج الفتق،[1]:30 ثم تم اكتشاف أدوية أخرى يمكنها صد هذه الاستجابة، مما يقلل من معدلات الوفيات بسبب الجراحة.
استخدام المخدر العام عن طريق الإستنشاق هو أكثر الطرق المستخدمة شيوعا في التخدير العام. ولكل نوع منها قوة خاصة ترجع إلى قدرتها على الذوبان في الزيت. ويرجع وجود هذه العلاقة إلى أن الأدوية ترتبط بتجاويف بروتينات موجودة في الجهاز العصبي المركزي، ومع ذلك فإن هناك العديد من النظريات الأخرى التي تفسر طريقة عمل التخدير العام. ويُعتقد أن التخدير بالإستنشاق يؤثر على أجزاء مختلفة من الجهاز العصبي المركزي. على سبيل المثال: عدم القدرة على الحركة بعد استنشاق المخدر يكون نتيجة تأثير المخدر على الحبل الشوكي، بينما المهدئات، والمنومات، وفقدان الذاكرة يتضمن العمل على مناطق معينة في المخ.[1]:515 وتتحدد قوة التخدير بالإستنشاق بالحد الأدنى لتركيزه في الحويصلات الهوائية (وهو عبارة عن نسبة جرعة المخدر التي سوف تمنع الاستجابة للمؤثرات المؤلمة في 50% من الأشخاص)، وكلما زادت هذه النسبة، كلما كان المخدر أقل قوة.

- بروبوفول، منوم
- إفيدرين، في حالة انخفاض ضغط الدم
- فنتانيل، لتسكين الألم
- أتراكيوريام، للإحصار العصبي العضلي
- جليكوبيرونيوم بروميد، لتقليل الإفرازات
المخدر المثالي هو المخدر الذي يؤدي إلى النوم، وفقدان الذاكرة، وتسكين الألم، وارتخاء العضلات دون تغيير غير مرغوب فيه في ضغط الدم، والنبض، والتنفس. وفي ثلاثينات القرن التاسع عشر بدأ الأطباء العمل على تقوية تأثير التخدير العام بالإستنشاق عن طريق حقن مخدر عام في الوريد معه، مما أدى إلى تقليل المخاطر الناجمة عن التخدير، وسرعة الاستفاقة. ومؤخرا تبين أن دمج الأدوية مع بعضها يؤدي إلى انخفاض احتمالات الوفاة خلال السبعة أيام الأولى بعد التخدير. على سبيل المثال: يمكن أن يستخدم بروبوفول (حقن) لبدء التخدير، ويستخدم فينتانيل (حقن) لصد الاستجابة للضغط، وميدازولام (حقن) لفقدان الذاكرة، وسيفوفلوران (استنشاق) أثناء العملية لاستمرار التأثير. ولقد طُورت العديد من الأدوية التي تُعطى عن طريق الوريد حديثا، بحيث يمكن استخدامها وتجنب التخدير العام عن طريق الإستنشاق تجنبا تاما.[1]:720
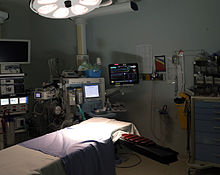
معدات[عدل]
تعتبر آلة التخدير هي الآلة الأساسية في نظام توصيل المخدر بالإستنشاق. حيث تحتوي على مبخرة، وجهاز تنفس اصطناعي، ونظام التنفس تحت التخدير، ونظام كسح نفايا الغازات، وأجهزة لقياس الضغط. وهدف آلة التخدير هو تزويد المريض بغاز مخدر تحت ضغط ثابت، وأكسجين للتنفس، والتخلص من ثاني أكسيد الكربون وغيره من نفايات غازات التخدير. بسبب أن مواد التخدير بالإستنشاق تسبب التهابات، فقد طورت العديد من قوائم الفحص المتنوعة للتأكد من أن الآلة جاهزة للاستخدام عن طريق التأكد من وجود عوامل أمان نشطة، وإزالة المخاطر الكهربائية.[3] بينما يتم إعطاء المخدر عن طريق الوريد في شكل جرعة ضخمة أو عن طريق الضخ بالتسريب. كما أن هناك العديد من الآلات الأصغر التي تستخدم لعمل مسلك هوائي اصطناعي، ومتابعة المريض. والقاسم المشترك بين الآلات الحديثة في هذا المجال هو استخدام أنظمة آمنة للفشل لتقليل الاحتمالات الكارثية للاستخدام الخاطيء للآلة.[4]
مراقبة[عدل]

يجب أن يخضع المرضى وهم تحت تأثير المخدر العام إلى المراقبة الفسيولوجية المستمرة للتأكد من الأمان. ولقد أنشأت الجمعية الأمريكية لأطباء التخدير في الولايات المتحدة مبادئ توجيهية لتحديد الحد الأدنى من المراقبة للمرضى الخاضعين للتخدير العام، أو التخدير الموضعي، أو المهدئات. وتتضمن المراقبة جهاز تخطيط القلب الكهربائي، ومتابعة معدل ضربات القلب، وضغط الدم، والغازات أثناء الشهيق والزفير، وتشبع الدم بالأكسجين، ودرجة الحرارة.[5] كما وضعت رابطة أطباء التخدير في المملكة المتحدة مباديء توجيهية للحد الأدنى للمراقبة مع التخدير العام، والموضعي. فالجراحات الصغيرة عامة تتضمن مراقبة معدل ضربات القلب، وتشبع الدم بالأكسجين، وضغط الدم، وتركيزات الإستنشاق والزفير لغاز الأكسجين، وثاني أكسيد الكربون، والمواد المستنشقة المخِدرة. وتتضمن المراقبة للعمليات الجراحية الجائرة: درجة الحرارة، ومعدل خروج البول، وضغط الدم، والضغط الوريدي المركزي، وضغط الشريان الرئوي، وضغط غلق الشريان الرئوي، والنتاج القلبي، والنشاط الدماغي، والوظيفة العصبية العضلية. بالإضافة إلى أنه يجب مراقبة البيئة المحيطة في غرفة العمليات مثل درجة الحرارة المحيطة، والرطوبة، وتراكم زفير المواد المخدرة المستنشقة التي يمكن أن تضر صحة الأفراد في غرفة العمليات.[6]
تهدئة[عدل]
تخلق المهدئات (تعود أيضا على التخدير الجزئي) نوعا من التنويم، والتهدئة، ومضادات للقلق، وفقدان للذاكرة، ومضادات للتشنجات، وخصائص مركزية لارتخاء العضلات. فيبدو المريض وكأنه نائم، ومرتخي، وفاقد للذاكرة، مما يمكن الطبيب من القيام بالإجراءات الطبية المؤلمة دون معاناة. وغالبا ما تعطى المهدئات مثل بينزوديازبين مع مسكن للألم (مثل: الناركوتيات، أو مخدر موضعي، أو كلاهما); لأن هذه المهدئات نفسها لا تخفف الألم بصورة كبيرة.[7] وبالنسبة للشخص الخاضع للتخدير فإنه يشعر بارتخاء عام، وفقدان للذاكرة، ومرور الوقت بسرعة. ويوجد الكثير من الأدوية التي تعطي هذا التأثير مثل: بنزوديازيبين، وبروبوفول، وبنتوثال الصوديوم، وكيتامين، والمخدِرات العامة بالإستنشاق. ومن مميزات المهدئات كمخدر عام أنها لا تتطلب دعم للمجرى الهوائي، أو التنفس (لا حاجة إلى تنبيب، أو تهوية ميكانيكية)، ولها تأثير أقل على نظام القلب والأوعية الدموية.[1]:736
تخدير موضعي[عدل]
عندما يوضع المخدر الموضعي على جزء من الجسم لمنع الإحساس بالألم يسمى تخدير ناحي، ويوجد منه أنواع عديدة سواء بالحقن في الأنسجة نفسها، أو في الوريد الذي يغذي المنطقة، أو حول العصب الذي يمد المنطقة بالإحساس فيما يسمى إحصار العصب وينقسم إلى إحصار طرفي، وإحصار مركزي.
وأنواع التخدير الناحي هي:[1]:926–931
- التخدير الارتشاحي: حيث يتم حقن كمية صغيرة من المخدر الموضعي في منطقة صغيرة لتوقيف أي إحساس (كما في حالة غلق تمزق أو تهتك في الأنسجة)، والتأثير يكون غالبا في الحال.
- إحصار العصب الطرفي: حيث يتم حقن المخدر الموضعي بالقرب من مكان العصب الذي يمد منطقة معينة من الجسم بالإحساس، وهناك اختلاف في سرعة بدأ عمل المخدر، وفترة استمرار تأثيره اعتمادا على فاعلية الدواء.
- تخدير وريدي ناحي (يسمى أيضا إحصار بيير): حيث يتم حقن مخدر موضعي مخفف بالتسريب في الوريد، مع ربط الطرف برباط ضاغط لمنع رجوع المخدر إلى خارج الطرف.
- إحصار العصب المركزي: حيث يتم حقن مخدر موضعي في جزء من الجهاز العصبي المركزي، أو حوله.
- تخدير موضعي: حيث تم صياغة المخدر الموضعي بطريقة خاصة ليتمكن من الانتشار خلال الغشاء المخاطي، أو الجلد لتعمل كطبقة بسيطة من المسكن في المنطقة (مثل لطخات خليط الليدوكائين، والبريلوكائين).
- تخدير انتباجي: يتم حقن كمية كبيرة من مخدر موضعي مخفف بدرجة كبيرة في نسيج تحت الجلد أثناء شفط الدهون.
- تخدير موضعي مجموعي: حيث تُعطى المخدِرات الموضعية عن طريق الفم، أو الوريد لتخفيف ألم الاعتلال العصبي.
إحصار عصبي[عدل]
إحصار العصب هو عبارة عن حقن مخدر موضعي حول العصب كبير القُطر الذي ينقل الإحساس من المنطقة بأكملها. وغالبا ما يستخدم إحصار الأعصاب في طب الأسنان، عندما يتم إحصار العصب الفكي السفلي عند القيام بأي إجراء طبي في الأسنان السفلية. ويتم تحديد العصب وموضع الإبرة باستخدام الموجات فوق الصوتية مع الأعصاب الأكبر قطرا (مثل إحصار عصب العضلة الأخمعية للأطراف العلوية أو العضلة القطنية للأطراف السفلية). حيث يقلل استخدام الموجات فوق الصوتية من معدلات حدوث مضاعفات، ويحسن جودة الأداء، ووقته، ووقت بداية الإحصار. ويجب وضع في الاعتبار الحد الأقصى لجرعة المخدر،[8] لأنه يلزم كمية كبيرة من المخدر الموضعي للتأثير على العصب. وعادة ما يستخدم إحصار العصب بالتسريب المستمر بعد الجراحة، مثل جراحات استبدال الركبة، والحوض، والكتف. ويمكن أن يصاحبه حدوث مضاعفات بمعدلات أقل[9] (خاصة المضاعفات العصبية) مقارنة بإحصار الجهاز العصبي المركزي.[1]:1639–1641
تخدير نصفي، وتخدير فوق الجافية، وتخدير عجزي[عدل]
تخدير الجهاز العصبي المركزي هو عبارة عن حقن مخدر موضعي حول الحبل الشوكي، لتسكين الألم في البطن، والحوض، والأطراف السفلية. وينقسم إلى تخدير نصفي (بالحقن في حيز تحت العنكبوتية)، وتخدير فوق الجافية (بالحقن خارج حيز تحت العنكبوتية في حيز فوق الجافية)، وتخدير عجزي (بالحقن في نهاية الحبل الشوكي). ويعتبر التخدير النصفي، وفوق الجافية هما الأكثر استخداما لإحصار الجهاز العصبي المركزي.
يتم التخدير النصفي عن طريق حقن المخدر دفعة واحدة، مما يوفر بداية سريعة لتأثيره، ونوعا من التخدير الحسي العميق باستخدام جرعات قليلة من المخدر، وعادة يكون مصحوبا بإحصار عصبي عضلي (فقد القدرة على التحكم في العضلات). ويستخدم في تخدير فوق الجافية كميات أكبر من المخدر يتم تسريبه عن طريق قسطرة مستقرة تسمح بزيادة المخدر عندما يبدأ زوال أثره. ولا يؤثر تخدير فوق الجافية على القدرة على التحكم في العضلات.
ولأن إحصار الجهاز العصبي المركزي يسبب توسيع شرياني ووعائي، فمن الشائع حدوث انخفاض شديد في ضغط الدم، ويكون الانخفاض بنسبة كبيرة بسبب الجانب الوريدي من الدورة الدموية المسئول عن 75% من حجم الدورة الدموية. ويكون التأثير الفسيولوجي بدرجة أكبر عندما يكون الإحصار أعلى الفقرة الصدرية الخامسة. وعادة ما يكون سبب عدم نجاح الإحصار هو عدم كفاية مضادات القلق أو المهدئات وليس فشل الإحصار نفسه.[1]:1611
التحكم في الألم الحاد[عدل]
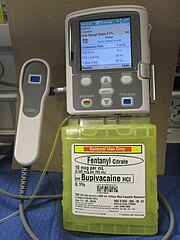
يحسن التحكم الجيد في الألم أثناء، وبعد الجراحة من صحة المريض عن طريق تقليل الضغط الفسيولوجي، واحتمالية الألم المزمن.[10] الإحساس بالألم هو عملية ديناميكية، أينما وُجِد مؤثر مؤلم فإنه يستحث الجهاز العصبي، مما يجعل التحكم في الألم صعب، أو يحوله إلى ألم مزمن. لذا فإن التحكم في الألم مسبقا بما يناسب الجراحة، والبيئة التي يعطى فيها، والمريض نفسه يساعد في تقليل الألم الحاد، والمزمن.[1]:2757
يتم تصنيف التحكم في الألم إما مسبقا، أو حسب الطلب. وتشمل أدوية تسكين الألم حسب الطلب على المسكنات الأفيونية، وأدوية مضاد التهاب لاستيرويدي، ويمكن أيضا استخدام أدوية جديدة مثل استنشاق أكسيد النيتروس،[11] وكيتامين.[12] ويمكن أن تعطى هذه الأدوية بواسطة الطبيب، أو بواسطة المريض عن طريق استخدام جهاز التحكم في تسكين الألم الذي أظهر تحكم في الألم أفضل، وأكثر إرضاء للمريض من الطرق التقليدية الأخرى.[13] ومن الوسائل الاستباقية الشائعة للتحكم في الألم قبل الجراحة: إحصار الجهاز العصبي المركزي بتخدير فوق الجافية،[14] أو إحصار العصب.[15] وقد وُجِد أن تخدير فوق الجافية يمكنه السيطرة على الألم (خصوصا أثناء الحركة) لفترة قد تصل إلى ثلاثة أيام بعد العملية، وتقلل فترة التنبيب بعد العملية إلى النصف تقريبا، كما أنه يقلل أيضا من طول فترة التهوية الميكانيكية، وخطر احتشاء عضلة القلب.[16]
مخاطر ومضاعفات[عدل]
تنقسم المخاطر والمضاعفات التي ترتبط بالتخدير إلى أمراض واضطرابات ناتجة من التخدير، أو أو قد تصل إلى الوفاة. ومن الصعب معرفة مدى ارتباط التخدير بمعدل الوفيات، والمرض بعد الجراحة. حيث أن صحة المريض قبل الجراحة، ودرجة التعقيد الجراحي تساهم أيضا في هذه المخاطر.

قبل معرفة التخدير في بداية القرن التاسع عشر، كان الضغط الفسيولوجي يتسبب في مضاعفات خطيرة، والكثير من الوفيات بسبب الصدمة. وكلما كانت الجراحة أسرع، كلما قل معدل حدوث المضاعفات. أدى ظهور التخدير إلى إمكانية إستكمال الجراحات الأكثر تعقيدا، والجراحات اللازمة لإنقاذ الحياة، وتقليل التوتر الفسيولوجي في الجراحة، ولكنه أضاف عنصر للخطر، حيث تم الإبلاغ عن أول حالة وفاة بسبب مخدر الإيثر بعد سنتين من اكتشافه.[18]
الأمراض التي يمكن أن يسببها التخدير يمكن أن تكون أمراض خطيرة (مثل: احتشاء عضلة القلب، والالتهاب الرئوي، والانصمام الرئوي، والفشل الكلوي، والخلل الإدراكي، والحساسية)، وأمراض أقل خطورة (مثل: الغثيان، والقيء، وإعادة الاحتجاز في المستشفى). وعادة ما يكون هناك نوعا من التداخل بين العوامل المساهمة في حدوث المرض أو الوفاة، وبين صحة المريض، والجراحة التي تم القيام بها، والتخدير. ولِفهم الخطر النسبي لكل عامل مساعد، يمكن أن نعتبر أن إجمالي معدل الوفيات الراجعة إلى أسباب متعلقة بصحة المريض هو 1:870، مقارنة بإجمالي معدل الوفيات الراجع إلى عوامل جراحية (1:2860)، أو للتخدير فقط (1:185.056)، مما يفسر أن صحة المريض هي العامل المساهم الأكبر في الوفاة. كما يمكن مقارنة هذه الإحصائيات مع الدراسات الأولى للوفيات أثناء التخدير منذ عام 1954، التي أقرت أن معدل الوفيات بسبب جميع هذه الأسباب هو 1:75، ومعدل الوفيات الراجع إلى التخدير وحده هو 1:2680.[1]:993 ولكن لايمكن الاعتماد على هذه المقارنات المباشرة بين إحصائيات الوفيات عبر الأزمنة والبلدان بسبب اختلاف تطبيق عوامل الخطر. ومع ذلك فهناك أدلة تثبت أن التخدير يزيد من درجة أمان الجراحة،[19] ولكن لم يتحدد بعد إلى أي درجة.[17]
ولقد تم إقرار العديد من العوامل الأخرى التي تساهم في الخطر النسبي مع الجراحة، والتخدير. على سبيل المثال:
- إجراء عملية لمريض في سن 60-70 عام يجعل المريض عرضة للخطر 2.32 مرة أكثر من الأشخاص تحت سن 60.
- حصول المريض على 3، أو 4، أو 5 درجات من مقياس الجمعية الأمريكية لأطباء التخدير يجعل المريض عرضة للخطر 10.65 مرة أكثر من شخص درجته 1، أو 2.
- السن: حيث ترتفع نسبة الخطر إلى 3.29 مرة أكثر فوق سن 80 عن تحت سن 60،
- الجنس: يكون معدل الخطر 0.77 مرة أقل في النساء،
- الحاجة الملحة للإجراء: 4.44 مرة أكثر في الحالات الطارئة.
- خبرة الطبيب الذي سيكمل الجراحة: (أقل من 8سنوات خبرة، أو أقل من 600حالة يجعل المريض عرضة للخطر 1.06 مرة أكثر من غيره).
- نوع التخدير: التخدير الموضعي أقل خطرا من التخدير العام.[1]:984
- التوليد: كلا من الولادة في سن صغير أو كبير يجعل المرأة عرضة للمضاعفات بدرجة كبيرة، لذا يجب وضع المزيد من الاحتياطات في الاعتبار.[1]:969–986
في 14ديسمبر 2016، أصدرت إدارة الغذاء، والدواء تحذيرا «بأن الاستخدام المتكرر، أو لفترات طويلة لأدوية التخدير العام، والمهدئات أثناء الجراحات، أو الإجراءات الطبية للأطفال أقل من 3سنوات، أو للحوامل خلال الثلاثة شهور الأخيرة من الحمل يمكن أن يؤثر على تطور أدمغة الأطفال».[20] وقد انتقدت جامعة النساء والتوليد الأمريكية هذا التحذير مشيرة إلى عدم وجود دليل مباشر فيما يخص الحوامل، وأنه من الممكن أن يثبط هذا التحذير من قدرة الأطباء على تقديم الرعاية الطبية الجيدة للنساء أثناء الحمل.[21] كما أدعى المرضى أن القيام بالتجارب الإكلينيكية العشوائية هو أمر غير أخلاقي، لأن التجارب على الحيوانات أثبتت وجود ضرر، وأظهرت الدراسات أن الاستخدام المفرط للتخدير يزيد من خطر حدوث صعف في القدرة على التعليم للأطفال الصغار بنسبة خطر 2.12.[22]
الاستفاقة[عدل]
يعرف الوقت الذي يلي زوال أثر المخدر مباشرة بالصحو، ويتطلب الصحو من التخدير العام، أو المهدئات المراقبة بعناية، لأنه يكون مازال هناك احتمالية لحدوث مضاعفات،[23] مثل: الغثيان، والقيء الذي يمكن أن يحدث بنسبة 9.8%، ولكن هذه المضاعفات تختلف باختلاف نوع التخدير، والإجراء الطبي. ويكون هناك حاجة إلى دعم المجرى الهوائي في 6.8% من الحالات، واحتباس البول (وهو أمر شائع بين الأشخاص أكبر من 50 عام)، وانخفاض ضغط الدم في 2.7% من الحالات، كما أنه من الشائع حدوث انخفاض في درجة حرارة الجسم، ورعشة، وتشوش مباشرة في الفترة ما بعد العملية نتيجة قلة الحركة وما يتبعه من نقص إنتاج الجسم للحرارة أثناء الإجراء الطبي.[1]:2707
الخلل الإدراكي بعد العملية، أو ما يعرف بتشوش ما بعد التخدير هو عبارة اضطراب في الإدراك يحدث بعد الجراحة، والذي يمكن وصفه على أنه هذيان الصحو (تشوش فترة ما بعد العملية مباشرة)، والخلل الإدراكي (نقص القدرة على الإدراك خلال الأسبوع الأول بعد العملية). وعلى الرغم من أن الهذيان، والخلل الإدراكي المبكر ما بعد العملية، والخلل الإدراكي طويل المدى منفصلون ولا يوجد ارتباط بينهم، إلا أن وجود الهذيان بعد العملية ينبئ بوجود خلل إدراكي مبكر بعد العملية.[24] ووفقا لدراسة حديثة أجريت في كلية ديفيد جيفن للطب في جامعة كاليفورنيا، فإن المخ يستخدم سلاسل من مجموعات أنشطة، أو محاور ليجد طريقه للعودة إلى الوعي. كما أن دكتور أندرو هدسون، وهو أستاذ مساعد في طب التخدير يقول أن الإفاقة من التخدير ليست فقط لمجرد زوال مفعول المخدر، ولكن المخ يجد طريقه للرجوع مرة أخرى خلال متاهة من النشاطات التي تسمح برجوع الوعي، ويمكن القول ببساطة بأن المخ يقوم بإعادة تشغيل نفسه.[25]
الخلل الإدراكي طويل المدى بعد العملية هو تدهو طفيف في الوظيفة الإدراكية، يمكن أن يستمر لأسابيع، أو شهور، أو أكثر. فقد لاحظ أقارب المريض بأنه قليل الانتباه، وضعيف الذاكرة، وأنه قد فقد الاهتمام بالنشاطات التي كان يفضلها مسبقا (كالكلمات المتقاطعة)، كما يلاحظ زملاؤه في العمل عدم قدرته على إستكمال المهام بنفس سرعته السابقة.[26] وهناك أدلة قوية تفيد بأن ذلك يحدث غالبا بعد جراحات القلب، وأن السبب الرئيسي في ذلك هو تكون صمامات صغيرة. كما أنه وجد أن الخلل الإدراكي يحدث أيضا بعد الجراحات غير القلبية لأسباب لم تتضح بعد، ولكن كبر السن هو أحد العوامل المساهمة في حدوثه.[1]:2805–2816
تاريخ[عدل]
كانت أول محاولة للتخدير العام في عصر ما قبل التاريخ عن طريق العلاج بالأعشاب. كما أن الكحوليات تعتبر واحدة من أقدم المهدئات التي كانت تستخدم في بلاد الرافدين منذ آلاف السنين.[27] ويقال أن السومريين هم أول من زرعوا، وحصدوا الخشخاش (منوم) في بلاد الرافدين منذ 3400 عام قبل الميلاد.[28][29]
امتلك المصريون القدماء بعض الآلات الجراحية،[30][31] بالإضافة إلى المسكنات الخام، والمهدئات التي تتضمن مستخلصات من فاكهة اليبروح (ماندراكورا).[32] وقد استخدم بيان كيو (بالصيني:扁鹊، ويد-جيلز:Pien Ch'iao) (طبيب باطني، وجراح صيني أسطوري) التخدير العام في الإجراءات الجراحية.
كما كانت تُستخدم فصائل متنوعة من المغد، الذي يحتوي على مواد فعالة تستخدم في التخدير عبر أوروبا، وآسيا، والأمريكتين. وفي القرن الثالث عشر في إيطاليا، استخدم تيودوريكو بورجوجنوني خلطات مشابهة مع مواد أفيوينة تحث على فقد الوعي، والعلاج بخليط من القلويدات التي اعتبرت عماد التخدير حتى القرن التاسع عشر. وقد كان يُستخدَم التخدير الموضعي في حضارة الإنكا، حيث كان يمضغ الشامانيون أوراق نبتة الكوكة، ثم يجرون عمليات في الجمجمة، ويبصقون في الجرح المؤلم لتخديره.[33] وتم استخلاص الكوكايين مؤخرا، وأصبح أول مخدر موضعي فعال، ولقد استخدم لأول مرة بواسطة كارل كولر باقتراح من سيغموند فرويد أثناء جراحة في العين عام 1884.[34] وكان الجراح الألماني أغسطس بيير أول من استخدم الكوكايين في التخدير النخاعي عام 1898.[35] وكان الجراح الروماني نيكولاي بيتتي (1860-1942) أول من استخدم الأفيونات كمسكن عن طريق النخاع، حيث قدم تجربته في باريس عام 1901.[36]

وقد ذكرت الكتابات العربية القديمة التخدير بالإستنشاق. وكانت هذه الفكرة هي أساس الإسفنج المنوم (إسفنج النوم) الذي عرضته مدرسة ساليرنو للطب في أواخر القرن الثاني عشر، وأوغو بورجنجنوني (1180-1258) في القرن الثالث عشر. وقد وصف هذا الإسفنج من قبل ابن أوغو، والجراحيين التابعين. وتعتمد هذه الطريقة على نقع الإسفنج في محلول من الأفيون، واليبروح، وبعض المواد الأخرى. ثم يتم تجفيف الإسفنج، وتخزينه، ويتم ترطيب الإسفنج مباشرة قبل العملية ووضعه تحت أنف المريض، فتسبب الأبخرة الناتجة فقد الوعي.
يعتبر الإيثر أشهر مادة مخدرة ، وقد تم تصنيعه في القرن الثامن.[37][37][38] ولكنه استغرق قرون لكي يتم تقدير أهميته في مجال التخدير. وقد لاحظ الطبيب باراسيلسوس في القرن السادس عشر عندما جعل الدجاج يستنشقه أنه ليس فقط يشعر بالنعاس، ولكنه أيضا لا يشعر بالألم. وقد بدأ استخدام الإيثر من قبل البشر في بداية القرن التاسع عشر، ولكن كعقاقير استجمامية فقط.[39]
وفي الوقت نفسه في عام 1772، اكتشف العالم الإنجليزي جوزيف بريستلي غاز أكسيد النيتروس. اعتقد الناس في البداية أنه قاتل، حتى لو كان بجرعات صغيرة، كما الحال مع أكسيد النيتروجين. ومع ذلك قرر المخترع والكيميائي البريطاني همفري ديفي تجربته على نفسه. ولدهشته وجد أن غاز أكسيد النيتروس يجعله يضحك، لذلك لُقب بالغاز المضحك. وقد كتب ديفي عن فاعلية أكسيد النيتروس وخصائصه التخديرية، ولكن لم يتابع أي أحد هذا الأمر في ذلك الوقت.
وقد لاحظ الطبيب الأمريكي كروفورد لونغ أن أصدقاءه لم يشعروا بالألم عندما جرحوا أنفسهم بينما كانوا يترنحون تحت تأثير الإيثر، وفكر في الحال في فاعليته في الجراحة. وكان أحد المشاركين في واحدة من تلك «حفلات سمر الإيثر» طالب يدعى جيمس فينابل، وكان لديه ورمان صغيران في حاجة إلى إستئصالهم، ولكنه كان خائفا من ألم الجراحة، فكان يؤجل العملية. فاقترح لونغ أن يقوم بهذه العملية بينما فينابل تحت تأثير الإيثر، ووافق فينابل. وفي 30مارس 1842 خضع فينابل لجراحة غير مؤلمة. ومع ذلك لم يعلن لونغ عن اكتشافه حتى عام 1849.[40]

قام هوراس ولز باستخدام التخدير بالإستنشاق لأول مرة في مستشفى ماساتشوستس العام في بوسطن عام 1845. ولكن لم يتم التخدير بأكسيد النيتروس بالشكل الصحيح، وصرخ المريض من شدة الألم.[41] في 16أكتوبر 1846، استخدم طبيب الأسنان وليم مورتون من بوسطن ثنائي إيثيل الإيثر لطلاب طب في نفس المكان.[42] ولقد دُعي مورتون _الذي لم يكن على علم بعمل لونغ السابق_ إلى مستشفى ماساتشوستس العام لتطبيق تقنيته الجديدة من أجل جراحة بلا ألم. وبعد أن قام مورتون بتخدير المريض، أزال الجراح جون كولينز وارن ورم من رقبة ادوارد جيلبرت أبوت. وحدث ذلك في مكان يسمى الآن بقبة الإيثر. وكان وارن أحد المشككين مسبقا، ولكنه أعجب بالأمر، وقال: «أيها السادة، هذا ليس هراء». واقترح الطبيب، والكاتب أوليفر وندل هولمز الأب في خطاب لمورتون بعد ذلك بوقت قصير تسمية هذه الحالة «بالتخدير»، والإجراء «بالبنج».[39]
حاول مورتون في البداية إخفاء طبيعة المادة المخدرة، وحصل على براءة اختراع أمريكية. ولكن أخبار المخدر الناجح انتشرت بسرعة في أواخر عام 1846. ثم قام العديد من الجراحين في أوروبا مثل: ليستون، وديفنباخ، وبيروغوف، وسايم بإجراء العديد من العمليات باستخدام الإيثر. وقد قام الطبيب الأمريكي المولد بووت بتشجيع طبيب الأسنان جيمس روبنسون من لندن، للقيام باستخدامه عند القيام بإجراء طبي في أسنان ملكة الجمال لونسديل. وفي نفس اليوم، في 19 ديسمبر 1846، في المصحة الملكية دومفريس في اسكتلندا، استخدم دكتور سكوت الإيثر لإجراء عملية جراحية.[43] كما كان أول استخدام للتخدير في نصف الكرة الجنوبي حدث في ونسيستون، في تسمانيا في نفس العام. وقد أدت عيوب الإيثر مثل القيء المفرط، وقابليته للاشتعال، والانفجار إلى إستبداله بالكلوروفورم في انجلترا.
اُكتُشف الكلوروفورم عام 1831 بواسطة الطبيب الأمريكي صمويل غوثري (1782-1848)، ثم بواسطة الفرنسي أوجين سوبيران بشكل مستقل بعد بضعة أشهر (1797-1859)، ثم جستس فون ليبج (1803-1873) في ألمانيا. وقد تم تسمية الكلوروفورم والتعرف على خصائصه الكيميائية في عام 1834 من قبل جان باتيست دوماس (1800-1884). وقد أشير إلى خصائصه المخدرة في وقت مبكر من عام 1847 من قبل ماري-جان-بيير فلورينس (1794-1867). ويرجع استخدام الكلوروفورم في التخدير إلى جيمس يونغ سيمبسون، الذي اكتشف خلال دراسة واسعة النطاق للمركبات العضوية فاعلية الكلوروفورم في 4نوفمبر 1847. وقد انتشر استخدامه بسرعة كبيرة، كما حصل على الموافقة الملكية في عام 1853، عندما أعطاه جون سنو إلى الملكة فيكتوريا أثناء ولادة الأمير ليوبولد. وللأسف، على الرغم من عدم قابليته للاشتعال، والانفجار مثل الإيثر، إلا أن الكلوروفورم ليس دواء آمن، خاصة عندما يعطى من قبل أشخاص غير مدربين (مثل: طلاب طب، والممرضيين، وأحيانا أفراد العامة الذين أجبروا على القيام بالتخدير في ذلك الوقت). مما أدى إلى العديد من الوفيات بسبب استخدامه، والتي كان من الممكن (بعد فوات الأوان) منعها. وقد تم تسجيل أول حالة وفاة بسبب الكلوروفورم في 28يناير 1848 بعد وفاة هانا جرينر.[44]
نشر جون سنو بداية من مايو 1848 وما بعده مقالات عن «التخدير بواسطة استنشاق الأبخرة» في الجريدة الطبية بلندن.[45] كما شارك بنفسه في إنتاج المعدات اللازمة للتخدير بالإستنشاق، فهو اليوم رائد آلات التخدير.[46]
ومن بين هذه المواد المخدرة المشهورة، مازال أكسيد النيتروس فقط هو الذي يتم استخدامه اليوم على نطاق واسع، وتم استبدال الكلوروفورم، والإيثر بالتخدير العام الأكثر أمانا، ولكنه أحيانا يكون أكثر تكلفة، وبالكوكايين كمخدر موضعي أكثر فاعلية ، مع تقليل فاعليته كمادة تؤدي إلى الإدمان.
الثقافة والمجتمع[عدل]
يستخدم معظم مقدمي الرعاية الصحية التخدير، ومع ذلك فإن كل مهنة صحية لها أشخاص متخصصون في مجالهم مثل: مجال الطب، والتمريض، وطب الأسنان. يعرف الأطباء المتخصصون في الرعاية ما قبل العمليات، ووضع خطة التخدير، وإعطاء المخدر للمريض بأطباء التخدير. ويتم إعطاء المخدر في المملكة المتحدة، وأستراليا، ونيوزيلاندا، وهونج كونج، واليابان بواسطة الأطباء. بينما يقوم الممرضون بالتخدير في 109 دولة.[47] وفي الولايات المتحدة، يقوم الأطباء بالتخدير منفردين بنسبة 35%، و55% بواسطة فريق للتخدير حيث يقوم طبيب التخدير بتوجيه مساعده، أو الممرضة ذات شهادة الخبرة. وحوالى 10% بواسطة الممرضة ذات شهادة الخبرة في التخدير بمفردها،[47][48][49] كما يمكن أن يوجد مساعدي أطباء التخدير، أو مساعدي الأطباء الذين يساعدوا في التخدير.[50]
مجتمعات خاصة[عدل]
هناك العديد من الظروف التي يمكن أن تحتاج إلى القيام بتغييرات في التخدير ليناسب هذه الظروف الخاصة، التي قد تكون متعلقة بالجراحة (مثل: جراحة القلب، وجراحة الأعصاب)، أو المريض (مثل: تخدير حديثي الولادة، أو كبار السن، أو مع السمنة، أو التوليد)، أو لظروف خاصة (مثل: خبطة، رعاية ما قبل النقل إلى المستشفى، أو الجراحة الروبوتية، أو البيئة القاسية).
انظر أيضًا[عدل]
- مادة حيوية
- تنظير داخلي
- جراحة أثناء النوم
- عقار (مادة كيميائية)
- تقييد طبي
- مسكن ألم
- تخدير موضعي
- جراحة ذاتية
المراجع[عدل]
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع غ ف Miller، Ronald D (2010). Erikson، Lars I؛ Fleisher، Lee A؛ Wiener-Kronish، Jeanine P؛ Young، William L (المحررون). Miller's Anesthesia Seventh edition. USA: Churchill Livingstone Elsevier. ISBN:978-0-443-06959-8.
- ^ Fitz-Henry, J (أبريل 2011). "The ASA classification and peri-operative risk". Annals of The Royal College of Surgeons of England. ج. 93 ع. 3: 185–187. DOI:10.1308/rcsann.2011.93.3.185a. PMC:3348554. PMID:21477427.
- ^ Goneppanavar، U؛ Prabhu، M (سبتمبر–أكتوبر 2013). "Anaesthesia Machine: Checklist, Hazards, Scavenging". Indian J Anaesth. ج. 57 ع. 5: 533–540. DOI:10.4103/0019-5049.120151. PMC:3821271. PMID:24249887.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Subrahmanyam M، Mohan S (سبتمبر 2013). "Safety Features in Anaesthesia Machine". Indian Journal of Anaesthesia. ج. 57 ع. 5: 472–480. DOI:10.4103/0019-5049.120143. PMC:3821264. PMID:24249880.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Standards for Basic Anesthetic Monitoring. Committee of Origin: Standards and Practice Parameters (Approved by the ASA House of Delegates on 21 October 1986, amended 20 October 2010 with an effective date of 1 July 2011) نسخة محفوظة 6 أبريل 2020 على موقع واي باك مشين.
- ^ Birks RJS، المحرر (مارس 2007). RECOMMENDATIONS FOR STANDARDS OF MONITORING DURING ANAESTHESIA AND RECOVERY 4th Edition (PDF). Association of Anaesthetists of Great Britain and Ireland. مؤرشف من الأصل (PDF) في 2017-08-29. اطلع عليه بتاريخ 2014-02-21.
- ^ Reddy S، Patt RB (نوفمبر 1994). "The benzodiazepines as adjuvant analgesics". Journal of Pain and Symptom Management. ج. 9 ع. 8: 510–4. DOI:10.1016/0885-3924(94)90112-0.
- ^ Walker KJ؛ وآخرون (أكتوبر 2009). "Ultrasound guidance for peripheral nerve blockade". Cochrane Database of Systematic Reviews. ج. 2009 ع. 4: CD006459. DOI:10.1002/14651858.CD006459.pub2. PMID:19821368.
- ^ Ullah H؛ وآخرون (أبريل 2014). "Continuous interscalene brachial plexus block versus parenteral analgesia for postoperative pain relief after major shoulder surgery". Cochrane Database of Systematic Reviews ع. 2: #. DOI:10.1002/14651858.CD007080.pub2. PMID:24492959.
- ^ Andreae, MH Andreae DA (17 أكتوبر 2012). "Local anaesthetics and regional anaesthesia for preventing chronic pain after surgery". Cochrane Database of Systematic Reviews. ج. 2012 ع. 10. DOI:10.1002/14651858.CD007105.pub2.
- ^ Klomp T؛ وآخرون (سبتمبر 2012). "Inhaled analgesia for pain management in labour". Cochrane Database of Systematic Reviews. ج. 12 ع. 9: CD009351. DOI:10.1002/14651858.CD009351.pub2.
- ^ Bell، Rae F؛ Dahl، Jørgen B؛ Moore، R Andrew؛ Kalso، Eija A (يناير 2006). "Perioperative ketamine for acute postoperative pain". Cochrane Database of Systematic Reviews. ج. 25 ع. 1: CD004603. DOI:10.1002/14651858.CD004603.pub2. PMID:16437490.
- ^ Hudcova J, McNicol E, Quah C, Lau J, Carr DB (18 Oct 2006). "Patient controlled opioid analgesia versus conventional opioid analgesia for controlling postoperative pain". Cochrane Database of Systematic Reviews. ج. 2006 ع. 4: CD003348. DOI:10.1002/14651858.CD003348.pub2. مؤرشف من الأصل في 1 مارس 2014. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Jones L؛ وآخرون (مارس 2012). "Pain management for women in labour: an overview of systematic reviews". Cochrane Database of Systematic Reviews. ج. 3: CD009234. DOI:10.1002/14651858.CD009234.pub2. PMID:22419342.
- ^ Novikova N؛ وآخرون (سبتمبر 2012). "Local anaesthetic nerve block for pain management in labour". Cochrane Database of Systematic Reviews. ج. 12 ع. 9: CD009351. DOI:10.1002/14651858.CD009351.pub2.
- ^ Nishimori M, Low JH, Zheng H, Ballantyne JC (11 يوليو 2012). "Epidural pain relief versus systemic opioid-based pain relief for abdominal aortic surgery". Cochrane Database of Systematic Reviews. ج. 2012 ع. 11: CD005059. DOI:10.1002/14651858.CD005059.pub3.
- ^ أ ب Lagasse, RS (ديسمبر 2002). "Anesthesia Safety: Model or Myth?". Anesthesiology. ج. 97 ع. 6: 1609–17. DOI:10.1097/00000542-200212000-00038. PMID:12459692.
- ^ Chaloner EJ، Ham RJ (أغسطس 2001). "Amputations at the London Hospital 1852–1857". Journal of the Royal Society of Medicine. ج. 94 ع. 8: 409–412. PMC:1281639. PMID:11461989.
- ^ Braz LG (أكتوبر 2009). "Mortality in Anesthesia: A Systematic Review". Clinics. Faculdade de Medicina of the University of São Paulo. ج. 64 ع. 10: 999–1006. DOI:10.1590/S1807-59322009001000011. PMC:2763076. PMID:19841708.
- ^ Food and Drug Administration "FDA Drug Safety Communication: FDA review results in new warnings about using general anesthetics and sedation drugs in young children and pregnant women", FDA Website, 14 December 2016. Retrieved on 3 January 2017. نسخة محفوظة 23 أبريل 2019 على موقع واي باك مشين.
- ^ American College of Obstetricians and Gynecologists "Practice Advisory: FDA Warnings Regarding Use of General Anesthetics and Sedation Drugs in Young Children and Pregnant Women", ACOG Website, 21 December 2016. Retrieved on 3 January 2017. نسخة محفوظة 10 يوليو 2017 على موقع واي باك مشين.
- ^ Kennerly Loutey "Anesthesia in Pregnant Women And Young Children: The FDA Versus ACOG", Website, Retrieved on 3 January 2017. نسخة محفوظة 14 يوليو 2018 على موقع واي باك مشين.
- ^ Whitaker DK، Booth H (مارس 2013). "Immediate post-anaesthesia recovery 2013: Association of Anaesthetists of Great Britain and Ireland". Anaesthesia. ج. 68 ع. 3: 288–97. DOI:10.1111/anae.12146. PMID:23384257.
- ^ Rudolph JL؛ وآخرون (سبتمبر 2008). "Delirium is associated with early postoperative cognitive dysfunction". Anaesthesia. ج. 63 ع. 9: 941–947. DOI:10.1111/j.1365-2044.2008.05523.x. PMC:2562627. PMID:18547292.
- ^ How brain 'reboots' itself to consciousness after anesthesia. Science Daily (June 18, 2014) نسخة محفوظة 27 فبراير 2018 على موقع واي باك مشين.
- ^ Deiner S، Silverstein JH (2009). "Postoperative delirium and cognitive dysfunction". British Journal of Anaesthesia. ج. 103 ع. Suppl 1: i41–i46. DOI:10.1093/bja/aep291.
- ^ Powell MA (1996). "Chapter 9: Wine and the vine in ancient Mesopotamia: the cuneiform evidence". The origins and ancient history of wine (Food and nutrition in history and anthropology) (ط. 1). Amsterdam: Gordon and Breach Publishers. ج. 11. ص. 96–124. ISBN:978-90-5699-552-2. مؤرشف من الأصل في 2020-03-12.
{{استشهاد بكتاب}}: الوسيط غير المعروف|المحررين=تم تجاهله (مساعدة) - ^ Evans، TC (1928). "The opium question, with special reference to Persia (book review)". Transactions of the Royal Society of Tropical Medicine and Hygiene. ج. 21 ع. 4: 339–340. DOI:10.1016/S0035-9203(28)90031-0. مؤرشف من الأصل في 2016-03-04. اطلع عليه بتاريخ 2010-09-18.
The earliest known mention of the poppy is in the language of the Sumerians, a non-Semitic people who descended from the uplands of Central Asia into Southern Mesopotamia ...
- ^ Booth M (1996). "The discovery of dreams". Opium: A History. London: Simon & Schuster, Ltd. ص. 15. ISBN:0-312-20667-4. مؤرشف من الأصل في 2020-03-12.
- ^ Ludwig Christian Stern (1889). Ebers G (ed.). Papyrus Ebers (بالألمانية) (1 ed.). Leipzig: Bei S. Hirzel. Vol. 2. OCLC:14785083. Archived from the original on 2016-06-10. Retrieved 2010-09-18.
- ^ Pahor، AL (1992). "Ear, nose and throat in ancient Egypt: Part I". Journal of Laryngology & Otology. ج. 106 ع. 8: 677–87. DOI:10.1017/S0022215100120560. PMID:1402355. مؤرشف من الأصل في 2016-08-20. اطلع عليه بتاريخ 2010-09-16.
- ^ Sullivan، R (1996). "The identity and work of the ancient Egyptian surgeon". Journal of the Royal Society of Medicine. ج. 89 ع. 8: 467–73. PMC:1295891. PMID:8795503.
- ^ Ruetsch، YA؛ Böni، T؛ Borgeat، A (2001). "From Cocaine to Ropivacaine: The History of Local Anesthetic Drugs". Current Topics in Medicinal Chemistry. ج. 1 ع. 3: 175–82. DOI:10.2174/1568026013395335. PMID:11895133.
- ^ Koller, K (1884). "Über die verwendung des kokains zur anästhesierung am auge" [On the use of cocaine for anesthesia on the eye]. Wiener Medizinische Wochenschrift (بالألمانية). 34: 1276–1309.
- ^ Bier, A (1899). "Versuche über cocainisirung des rückenmarkes" [Experiments on the cocainization of the spinal cord]. Deutsche Zeitschrift für Chirurgie (بالألمانية). 51 (3–4): 361–9. DOI:10.1007/BF02792160.
- ^ Brill، S؛ Gurman، GM؛ Fisher، A (2003). "A history of neuraxial administration of local analgesics and opioids". European Journal of Anaesthesiology. ج. 20 ع. 9: 682–9. DOI:10.1017/S026502150300111X. PMID:12974588.
- ^ أ ب Toski, Judith A؛ Bacon, Douglas R؛ Calverley, Rod K (2001). The history of Anesthesiology (ط. 4). Lippincott Williams & Wilkins. ص. 3. ISBN:978-0-7817-2268-1.
{{استشهاد بكتاب}}:|عمل=تُجوهل (مساعدة) - ^ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. (12 نوفمبر 2008). McGraw-Hill's PCAT. McGraw-Hill. ص. 39. ISBN:978-0-07-160045-3. مؤرشف من الأصل في 2020-03-12.
- ^ أ ب Fenster، JM (2001). "Power Struggle". Ether Day: The Strange Tale of America's Greatest Medical Discovery and the Haunted Men Who Made It. New York: HarperCollins. ص. 106–16. ISBN:978-0-06-019523-6. مؤرشف من الأصل في 2020-01-10.
- ^ Long، CW (1849). "An account of the first use of Sulphuric Ether by Inhalation as an Anesthetic in Surgical Operations". Southern Medical and Surgical Journal. ج. 5: 705–713.
- ^ "Miniature Portrait of Horace Wells". National Museum of American History, Smithsonian Institution. مؤرشف من الأصل في 2009-07-05. اطلع عليه بتاريخ 2008-06-30.
- ^ Morkel، H (16 أكتوبر 2013). "The painful story behind modern anesthesia". pbs.org. مؤرشف من الأصل في 2017-09-11.
- ^ Baillie، Thomas W. (1965). "The first European trial of anaesthetic ether: The Dumfries claim". British Journal of Anaesthesia. ج. 37: 952–957. DOI:10.1093/bja/37.12.952.
- ^ Wawersik، J. (1 يناير 1997). "History of chloroform anesthesia". Anaesthesiologie Und Reanimation. ج. 22 ع. 6: 144–152. PMID:9487785.
- ^ Zorab، John (يونيو 1992). "On Narcotism by the Inhalation of Vapours by John Snow MD". Journal of the Royal Society of Medicine. ج. 85 ع. 6: 371.
- ^ "Anesthesia LAND". patinaa.blogfa.com. مؤرشف من الأصل في 2018-11-19. اطلع عليه بتاريخ 2016-12-02.
- ^ أ ب McAuliffe، MS؛ Henry، B (2010). "Nurse anesthesia worldwide: practice, education and regulation" (PDF). Downloads. Silver Spring, Maryland: International Federation of Nurse Anesthetists. مؤرشف من الأصل (PDF) في 2012-02-20. اطلع عليه بتاريخ 2012-06-13.
- ^ Abenstein، JP؛ Long، KH؛ McGlinch، BP؛ Dietz، NM (2007). "Is Physician Anesthesia Cost-Effective?". Anesthesia & Analgesia. ج. 98 ع. 3: 750–7. DOI:10.1213/01.ANE.0000100945.56081.AC. PMID:14980932.
- ^ Rosenbach، ML؛ Cromwell، J (2007). "When do anesthesiologists delegate?". Medical Care. ج. 27 ع. 5: 453–65. DOI:10.1097/00005650-198905000-00002. PMID:2725080.
- ^ "Five facts about AAs". American Academy of Anesthesiologist Assistants. مؤرشف من الأصل في 2006-09-26. اطلع عليه بتاريخ 2010-11-25.
| تخدير في المشاريع الشقيقة: | |
| |